Da bi prednosti imunoterapije doneli većem broju pacijenata, naučnici su se okrenuli sintetičkoj biologiji, novoj oblasti proučavanja koja nastoji da redizajnira prirodu novim i korisnijim funkcijama. Istraživači su razvili novu vrstu terapije koja direktno pacijentima daje novi set T ćelija dizajniranih da napadnu tumore: himerične T ćelije receptora antigena, ili skraćeno CAR-T ćelije.
Kao onkološki lekar i istraživač, verujem da terapija ćelijama CAR-T ima potencijal da transformiše lečenje raka. Već se koristi za lečenje limfoma i multiplog mijeloma, i pokazao je izuzetne stope odgovora tamo gde drugi tretmani nisu uspeli.
Međutim, sličan uspeh protiv određenih vrsta tumora kao što su rak pluća ili pankreasa se sporije razvija zbog jedinstvenih prepreka koje postavljaju T ćelijama. U našem nedavno objavljenom istraživanju, moje kolege i ja smo otkrili da bi dodavanje sintetičkog kola CAR-T ćelijama potencijalno moglo da im pomogne da zaobiđu barijere koje tumori postavljaju i poboljšaju njihovu sposobnost da eliminišu više vrsta raka.
Kako funkcioniše CAR-T ćelijska terapija?
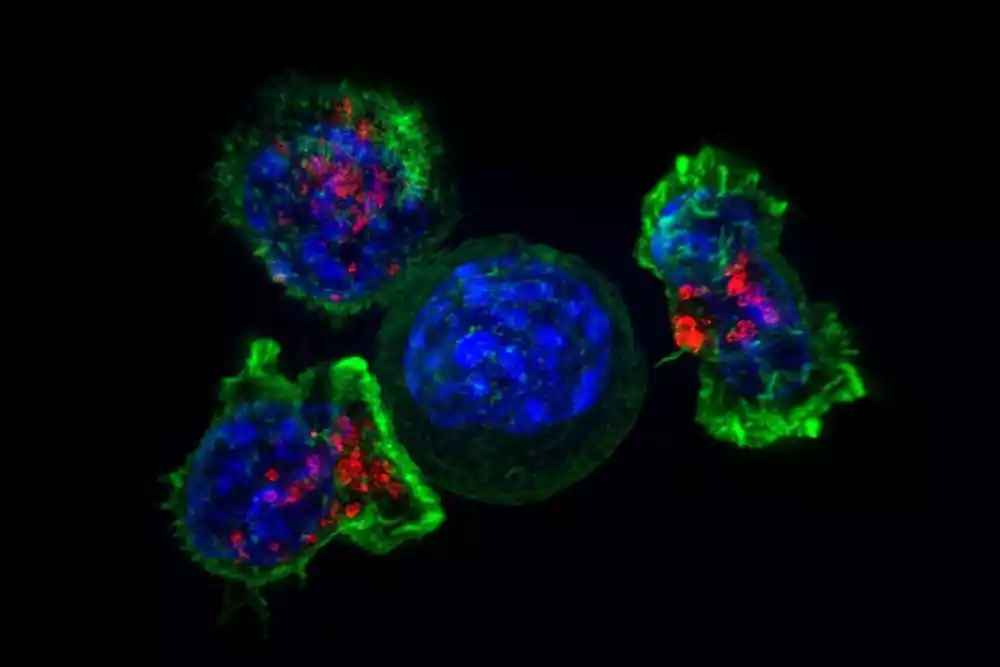
Terapija CAR-T ćelijama počinje tako što lekari izoluju T ćelije pacijenta iz uzorka njihove krvi. Ove T ćelije se zatim vraćaju u laboratoriju, gde su genetski konstruisane da proizvedu himerni antigen receptor, ili CAR.
CAR su sintetički receptori posebno dizajnirani da preusmere T ćelije sa svojih uobičajenih ciljeva da ih prepoznaju i usavrše tumorske ćelije. Na spoljašnjoj strani CAR-a nalazi se vezivo koje omogućava T ćeliji da se zalepi za ćelije tumora. Vezivanje za tumorsku ćeliju aktivira konstruisanu T ćeliju da ubije i proizvodi inflamatorne proteine citokina koji podržavaju rast i funkciju T ćelija i povećavaju njihove sposobnosti ubijanja raka.
Ove CAR-T ćelije se zatim stimulišu da se podele na veliki broj tokom sedam do 10 dana, a zatim se vraćaju pacijentu putem infuzije. Proces infuzije se obično odvija u bolnici gde kliničari mogu da prate znake preaktivnog imunološkog odgovora na tumore, što može biti smrtonosno za pacijenta.
Ubijanje T ćelija u čvrste tumore
Dok je terapija ćelijama CAR-T bila uspešna kod karcinoma krvi, suočila se sa preprekama u borbi protiv onih koji se nazivaju čvrsti tumorski karcinomi kao što su rak pankreasa i melanom. Za razliku od karcinoma koji počinje u krvi, ove vrste raka rastu u čvrstu masu koja stvara mikrookruženje molekula, ćelija i struktura koje sprečavaju T ćelije da uđu u tumor i izazovu imuni odgovor. Ovde, čak i CAR-T ćelije dizajnirane da specifično ciljaju jedinstveni tumor pacijenta nisu u mogućnosti da mu pristupe, potiskujući njihovu sposobnost da ubijaju tumorske ćelije.
Za zajednicu sintetičke biologije, neuspesi prve generacije CAR-T ćelijske terapije bili su poziv na akciju za razvoj nove porodice sintetičkih receptora za rešavanje jedinstvenih izazova koje postavljaju čvrsti tumori. Godine 2016, moje kolege u laboratoriji Lim na Kalifornijskom univerzitetu u San Francisku razvile su novi sintetički receptor koji bi mogao da dopuni prvi CAR dizajn. Ovaj receptor, nazvan sintetički Notch receptor, ili sinNotch, zasnovan je na prirodnom obliku Notch-a u telu, koji igra važnu ulogu u razvoju organa kod mnogih vrsta.
Slično kao CAR, spoljašnjost sinNotch-a ima vezivo koje omogućava T ćelijama da se zalepe za ćelije tumora. Za razliku od CAR-a, unutrašnjost sinNotch-a ima protein koji se oslobađa kada se T ćelija veže za tumor. Ovaj protein, ili faktor transkripcije, omogućava istraživačima da bolje kontrolišu T ćeliju indukujući je da proizvodi određeni protein.
Na primer, jedna od najkorisnijih primena sinNotch-a do sada je bila njegova upotreba kako bi se osiguralo da se projektovane T ćelije aktiviraju samo kada su vezane za tumorsku ćeliju, a ne zdrave ćelije. Pošto se CAR može vezati i za tumorske i za zdrave ćelije i indukovati T ćelije da ubiju oba, moje kolege su konstruisale T ćelije koje se aktiviraju samo kada su i sinNotch i CAR vezani za tumorsku ćeliju. Pošto T ćelije sada zahtevaju i CAR i sinNotch receptore da prepoznaju tumore, ovo povećava preciznost ubijanja T ćelija.
Pitali smo se da li možemo da koristimo sinNotch da poboljšamo aktivnost CAR-T ćelija protiv čvrstih tumora tako što ćemo ih podstaći da proizvode više inflamatornih citokina, kao što je IL-2, koji im omogućavaju da ubijaju tumorske ćelije. Istraživači su učinili mnogo pokušaja da obezbede dodatni IL-2 kako bi pomogli CAR-T ćelijama da očiste tumore. Ali pošto su ovi citokini veoma toksični, postoji ograničenje koliko IL-2 pacijent može bezbedno da toleriše, ograničavajući njihovu upotrebu kao leka.
Tako smo dizajnirali CAR-T ćelije da proizvode IL-2 koristeći sinNotch. Sada, kada CAR-T ćelija naiđe na tumor, ona proizvodi IL-2 unutar tumora umesto izvan njega, izbegavajući nanošenje štete okolnim zdravim ćelijama. Pošto je sinNotch u stanju da zaobiđe barijere koje tumori postavljaju, on je u stanju da pomogne T ćelijama da pojačaju i održe količinu IL-2 koju mogu da naprave, omogućavajući T ćelijama da nastave da funkcionišu čak i u neprijateljskom mikrookruženju.
Testirali smo naše CAR-T ćelije modifikovane sa sinNotch na miševima sa rakom pankreasa i melanomom. Otkrili smo da su CAR-T ćelije sa sinNotch-indukovanim IL-2 bile u stanju da proizvedu dovoljno dodatnog IL-2 da prevaziđu odbrambene barijere tumora i da se potpuno aktiviraju, potpuno eliminišući tumore. Dok su svi miševi koji su primali sinNotch modifikovane CAR-T ćelije preživeli, nijedan od miševa samo CAR-T nije.
Štaviše, naše sinNotch modifikovane CAR-T ćelije su bile u stanju da pokrenu proizvodnju IL-2 bez izazivanja toksičnosti za zdrave ćelije u ostatku tela. Ovo sugeriše da naš metod projektovanja T ćelija za proizvodnju ovog toksičnog citokina samo tamo gde je to potrebno može pomoći u poboljšanju efikasnosti CAR-T ćelija protiv raka uz smanjenje neželjenih efekata.
Sledeći koraci
Ostaju fundamentalna pitanja o tome kako će se ovaj rad na miševima prevesti na ljude. Naša grupa trenutno sprovodi više studija o korišćenju CAR-T ćelija sa sinNotch-om za proizvodnju IL-2, sa ciljem da uđe u klinička ispitivanja u ranoj fazi kako bi se ispitala njegova bezbednost i efikasnost kod pacijenata sa karcinomom pankreasa.