Takozvani patološki protein koji je dugo bio povezan sa Parkinsonovom bolešću pronađen je u novoj studiji da pokrene ćelije da povećaju sintezu proteina, događaj koji na kraju ubija podskup moždanih ćelija koje odumiru u ovom neurodegenerativnom stanju.
Istraživači sa Medicinskog fakulteta Univerziteta Džons Hopkins koji su sproveli studiju kažu da nalazi nude potencijalne nove ciljeve za lečenje Parkinsonove bolesti, koja pogađa oko 1% američke populacije starije od 60 godina i nema lek.
Nalazi su objavljeni u časopisu Science Translational Medicine. „Parkinsonova bolest ima veliki uticaj na kvalitet života pacijenata, ali i njihovih staratelja i voljenih“, kaže vođa studije Ted M. Davson, MD, Ph.D., profesor na Odeljenju za neurologiju i direktor Instituta za Ćelijsko inženjerstvo na Medicinskom fakultetu Univerziteta Džons Hopkins.
„Nadamo se da će ovakva istraživanja pružiti mehaničke, molekularne terapije koje zapravo mogu usporiti ili zaustaviti napredovanje Parkinsonove bolesti.“
Simptomi Parkinsonove bolesti, uključujući razne motoričke i kognitivne deficite koji se vremenom pogoršavaju, rezultat su smrti neurona koji proizvode hemijski glasnik dopamin. Trenutni tretmani lekovima kao što je L-dopa prvenstveno se fokusiraju na zamenu dopamina izgubljenog kada ovi dopaminergički neuroni umru.
Tokom protekle dve decenije, istraživači su povezivali smrt ovih ćelija sa prisustvom patološkog oblika alfa-sinukleina, normalnog proteina koji ima u izobilju u moždanom tkivu. Međutim, nejasno je kako patološki alfa-sinuklein uzrokuje smrt dopaminergičkih neurona. Da bi odredili njegovu ulogu, Doson i njegove kolege su koristili obeležavanje blizine zajedno sa masenom spektrometrijom da identifikuju proteine koji bi mogli da stupe u interakciju sa patološkim alfa-sinukleinom i kod miša i kod modela laboratorijskih ćelija Parkinsonovih neurona.
Identifikovali su 100 takvih proteina koji su se preklapali između ova dva modela. Kada su istraživači grupisali proteine prema funkciji, otkrili su da većina igra ulogu u obradi ribonukleinske kiseline (RNK) i započinjanju translacije – kritičnim procesima koje ćelije koriste za stvaranje novih proteina.
Već je poznato da nekoliko proteina radi sa metom rapamicina (mTOR), koji ima dvostruku ulogu u regulisanju proizvodnje proteina i razbijanju proteina.
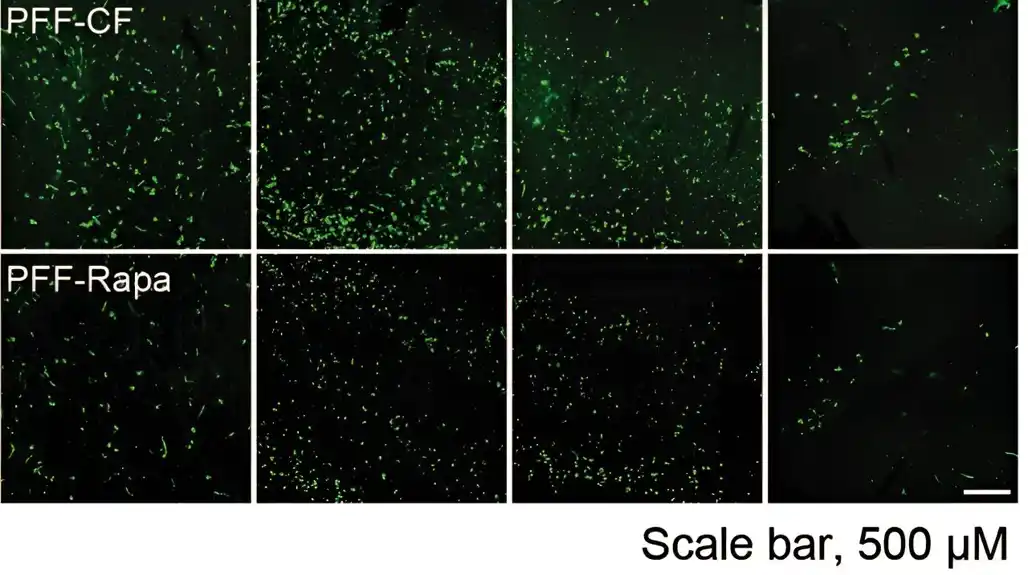
Eksperimenti na miševima kojima se genetski manipuliše da bi se prekomerno izrazio patološki oblik alfa-sinukleina pokazali su da je on zaista prouzrokovao ćelije da povećaju sintezu proteina aktiviranjem mTOR-a.
Ovaj proces je pokrenut, kažu istraživači, kada se patološki alfa-sinuklein vezao za drugi protein, kompleks tuberozne skleroze 2 (TSC2), sprečavajući ga da se poveže sa još jednim proteinom, TSC1, koji drži mTOR pod kontrolom.
Tretiranje genetski modifikovanih miševa rapamicinom, lekom koji cilja na mTOR, ne samo da je sprečilo prekomernu proizvodnju proteina kod miševa sa stanjem poput Parkinsonove bolesti, već je i olakšalo neke od sporih, zaustavljenih pokreta i slabe snage hvata koji su obeležja Parkinsonove bolesti kod ljudi. .
Doson kaže da još uvek nije jasno kako bi povećana proizvodnja proteina mogla da naškodi dopaminergičkim neuronima – proteini mogu začepiti ključne ćelijske puteve, ili specifični proteini proizvedeni u višku mogu biti štetni za ćelije. On i njegove kolege planiraju da istraže to pitanje u budućim istraživanjima.
U međuvremenu, kaže on, nalazi ukazuju na nove ciljeve za lečenje Parkinsonove bolesti. Istraživači mogu, na primer, da razviju lekove koji deluju kao rapamicin – koji se trenutno koristi kao lek protiv odbacivanja i protiv raka – ali rade posebno u mozgu kako bi sačuvali dopaminergičke neurone, štedeći pacijente nepotrebnih neželjenih efekata širom tela. Ili, možda je moguće ciljati TSC2 da bi se proizveo sličan efekat.