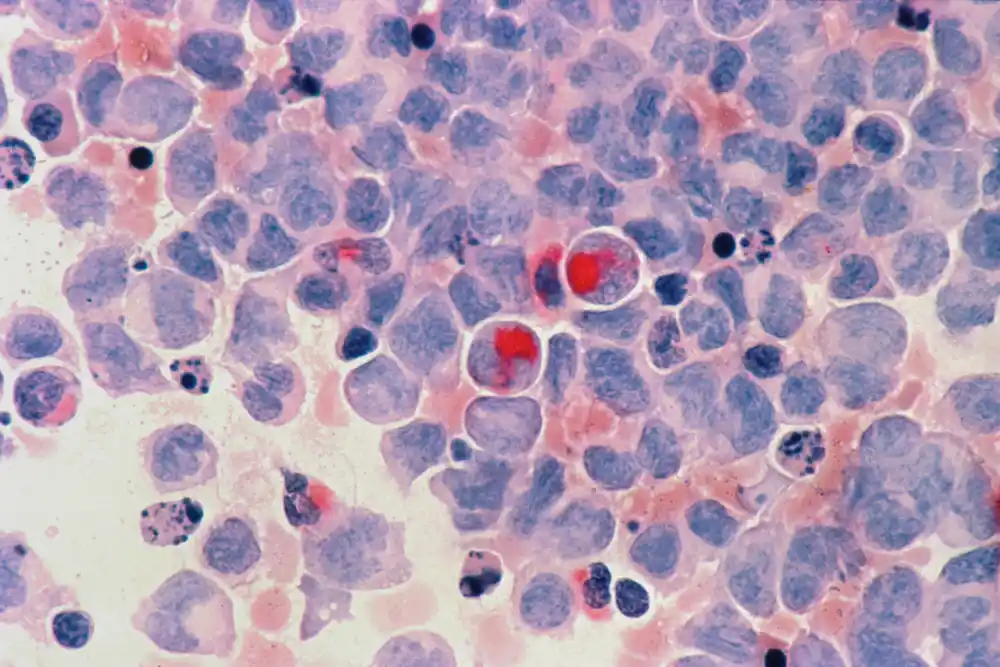
Uprkos tome što ima ukupnu stopu preživljavanja od 94%, akutna limfoblastna leukemija B-ćelija (B-ALL), najčešći rak u detinjstvu, može se pokazati kao izazovna za lečenje, sa preživljavanjem među relapsima ili rezistentnim slučajevima između 30-50%.
U nedavnom radu Dečje istraživačke bolnice St. Jude, naučnici su otkrili koje tumorske ćelije se opiru tretmanu i zašto. Ovo je omogućilo racionalan dizajn kombinovane terapije koja je bolje kontrolisala visokorizične podtipove B-ALL u modelima miševa. Nalazi su objavljeni danas u Cancer Cell.
„Pronašli smo novo objašnjenje B-ALL osetljivosti na asparaginazu, koja je jedan od najčešće korišćenih lekova za ovu bolest“, rekao je stariji ko-korespondent autor Jun J. Iang, dr., Odeljenje za farmaciju St. Jude i potpredsednik za farmaceutske nauke. „Iako asparaginaza postoji skoro 50 godina, način na koji koristimo ovaj lek za SVE ostaje neprecizan. To je delom zato što još uvek ne razumemo u potpunosti mehanizam kojim ona ubija ćelije leukemije.“
Naučnici su pokazali da je kombinovanje klasičnog leka asparaginaze (hemoterapija) sa novijim lekom, venetoklaksom (terapija ciljanom BCL-2), najefikasnije u lečenju B-ALL na laboratorijskim modelima. Kombinacija je smanjila broj ćelija leukemije više nego bilo koji lek sam i delovala je brže. Poboljšani efekti su bili dosledni kod tri različita visokorizična podtipa ovog raka.
„Ovo otkriće je omogućeno biološkom analizom jednoćelijskog sistema razvoja B ćelija i integracijom sa profilisanjem osetljivosti na lekove B-ALL i podacima o sekvenciranju masovne RNK“, rekao je ko-korespondentni autor Jiiang Iu, dr. sc, Odeljenje St. Jude privremene katedre računarske biologije. „Naša analiza jednoćelijske mreže otkrila je protein BCL-2 kao skrivenu ranjivost u fazi razvoja tumora otpornog na asparaginazu.“
„Primena asparaginaze zajedno sa venetoklaksom može smanjiti rizik od recidiva ALL-a, što je glavni razlog neuspeha lečenja“, rekao je koautor Ching-Hon Pui, MD, Odeljenje za onkologiju St. Jude, Fahad Nassar Al-Rashid, predsedavajući za istraživanje leukemije. „U idealnom slučaju, cilj nam je da venetoklaks pojača svojstva asparaginaze protiv leukemije, a da istovremeno drži nivoe toksičnosti pod kontrolom. Ovi koncepti zahtevaju dalja istraživanja u budućim kliničkim ispitivanjima.“
Venetoclak je već odobren od strane Uprave za hranu i lekove za upotrebu kod drugih pedijatrijskih karcinoma, što ga čini atraktivnim kandidatom. Lek se pokazao bezbednim u tim okruženjima, otvarajući put za buduće odobrenje u lečenju B-ALL. Najveća prepreka je bilo razumevanje kako venetoklak deluje sa asparaginazom da zaustavi leukemiju B-ćelija.
B-ALL je rak koji potiče od belih krvnih zrnaca zvanih B ćelije. U normalnim okolnostima, B ćelije se razvijaju od nezrele do potpuno zrele, prolazeći kroz osam koraka. Kod kancera, ćelije se mogu zaglaviti u srednjoj fazi razvoja. U srodnoj bolesti, T-ćelijska akutna limfoblastna leukemija,
Jang i Ju su ranije otkrili, kao što je objavljeno u Nature Cancer 2021, da razvojna faza u kojoj se T ćelije zaglavljuju određuje njihovu osetljivost na terapeutike. Istraživači su želeli da shvate šta je nateralo ćelije u određenoj fazi da reaguju na koji lek, nadajući se da će takvo razumevanje predstavljati nove terapeutske mogućnosti.
„U ovom slučaju, otkrili smo da su tumorske B ćelije zaglavljene u dve glavne faze“, rekao je Ju. „Jedna je ranija faza koja je otpornija na asparaginazu i druga kasnija faza koja je osetljivija na nju.
Iu je pogledao podatke o ekspresiji gena iz stotina hiljada pojedinačnih kancerogenih B ćelija da bi razumeo šta je kod njih drugačije. Nakon što je identifikovao dve dominantne faze razvoja B-ćelija B-ALL, pre-pro-B (rano) i pro-B (kasno), njegova laboratorija je tražila gene koji su pojačano regulisani u rezistentnim ranim ćelijama da bi identifikovala potencijalne ranjivosti za terapeutski cilj. .
„Protein BCL-2 je privukao našu pažnju, jer se čini da je pokretač otpornosti na asparaginazu u ćelijama leukemije sa pre-pro-B karakteristikama“, rekao je Ju.
Protein B ćelijskog limfoma 2 (BCL-2) je protein uključen u smrt ćelije. Ćelije raka ga koriste da izbegnu sisteme koji ih obično uzrokuju samouništenje. Protein je takođe nizvodno od mTOR-a, proteina ciljanog asparaginazom. Nalazi su pokazali da se BCL-2 aktivirao u ćelijama raka otpornim na taj lek. Taj odnos otpora motivisao je naučnike da isprobaju venetoklaks, koji cilja na protein BCL-2, u kombinovanom pristupu.
„Kada dodate asparaginazu, pogađate mTOR signalizaciju“, rekao je Jang. „Zauzvrat, to povećava aktivnost BCL-2, čineći ćelije osetljivijim na venetoklaks.“
Rad ima implikacije i na druge vrste raka, jer je nepravilan razvoj u osnovi mnogih oblika bolesti. Sekvenciranje i analiza jednoćelijskih gena mogu pružiti slične mogućnosti za poboljšanje terapija u tim kontekstima.
„Pokazali smo da razvojno zaustavljanje ćelija raka može da ih učini osetljivim na određene lekove“, rekao je Jang. „Kada odredimo uključene puteve, možemo pronaći nove kombinacije lekova za poboljšanje ishoda lečenja.“