Nova tehnika snimanja koju su razvili inženjeri sa Vašingtonskog univerziteta u Sent Luisu može naučnicima dati mnogo bliži pogled na sklopove fibrila – gomile peptida koji uključuju amiloid beta, koji je najviše povezan sa Alchajmerovom bolešću.
Ovi sklopovi unakrsnih β fibrila su takođe korisni gradivni blokovi u dizajnerskim biomaterijalima za medicinske primene, ali je zabrinjavajuća njihova sličnost sa njihovim amiloidnim beta rođacima, čije su zamršenosti simptom neurodegenerativne bolesti. Istraživači žele da nauče kako su različite sekvence ovih peptida povezane sa njihovom različitom toksičnošću i funkcijom, kako za peptide koji se pojavljuju u prirodi, tako i za njihove sintetički konstruisane rođake.
Sada, naučnici mogu dovoljno dobro da pogledaju sklopove fibrila da vide da postoje značajne razlike u tome kako se sintetički peptidi slažu u poređenju sa amiloidnim beta. Ovi rezultati potiču iz plodne saradnje između glavnog autora Matthev Lev-a, vanrednog profesora elektrotehnike i sistemskog inženjeringa, i Jai Rudra, vanrednog profesora biomedicinskog inženjerstva, u VashU-ovoj školi za inženjerstvo McKelvei.
„Mi konstruišemo mikroskope kako bismo omogućili bolja merenja u nanorazmeri kako bi nauka mogla da krene napred“, rekao je Lu.
U radu koji je nedavno objavljen u ACS Nano, Lev i njegove kolege navode kako su koristili nilsku crvenu hemijsku sondu da osvetle unakrsne β fibrile. Njihova tehnika, nazvana mikroskopija orijentacije i lokalizacije jednog molekula (SMOLM), koristi bljeskove svetlosti iz Nilskog crvenog da vizualizuje strukture vlakana formiranih od sintetičkih peptida i beta amiloida.
Zaključak: Ovi sklopovi su mnogo komplikovaniji i heterogeniji nego što se očekivalo. To je dobra vest jer znači da postoji više od jednog načina za bezbedno slaganje proteina. Uz bolja merenja i slike sklopova fibrila, bioinženjeri mogu bolje razumeti pravila koja diktiraju kako gramatika proteina utiče na toksičnost i biološku funkciju, što dovodi do efikasnijih i manje toksičnih terapija.
Prvo, naučnici treba da vide razliku između njih, što je veoma izazovno zbog male veličine ovih skupova.
„Helikovito uvijanje ovih vlakana nemoguće je uočiti pomoću optičkog mikroskopa, ili čak nekih mikroskopa super-rezolucije, jer su te stvari jednostavno premale“, rekao je Lev.
Sa tehnologijom snimanja visoke dimenzije koja je razvijena u Levovoj laboratoriji u poslednjih nekoliko godina, oni su u stanju da vide razlike.
Tipičan fluorescentni mikroskop koristi fluorescentne molekule kao sijalice da istakne određene aspekte biološke mete. U slučaju ovog rada, koristili su jednu od tih sondi, nilsku crvenu, kao senzor za ono što je oko nje. Dok nilska crvena nasumično istražuje svoju okolinu i sudara se sa fibrilima, emituje bljeskove svetlosti koje oni mogu da izmere da bi odredili gde se nalazi fluorescentna sonda i njenu orijentaciju. Na osnovu tih podataka, oni mogu da sastave punu sliku projektovanih fibrila koji se slažu veoma različito od prirodnih, kao što je amiloid beta.
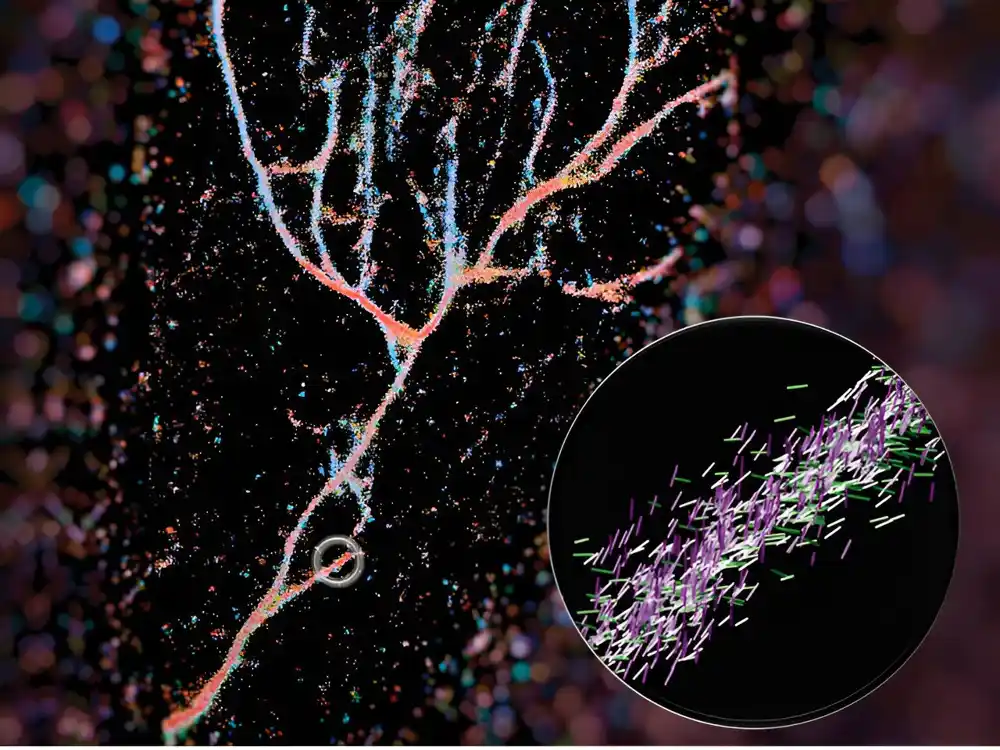
Njihova slika ovih fibrilnih sklopova napravila je naslovnicu ACS Nano, a sastavio ju je prvi autor Veiian Zhou, koji je bojom označio sliku na osnovu toga gde su nilske crvene boje pokazivale. Dobijena slika je plavičasto-crveni tečni sklop peptida koji izgleda kao rečna dolina.
Istraživači planiraju da nastave da razvijaju tehnike kao što je SMOLM kako bi otvorili nove puteve proučavanja bioloških struktura i procesa na nanoskali.
„Vidimo stvari koje ne možete da vidite sa postojećom tehnologijom“, rekao je Lu.