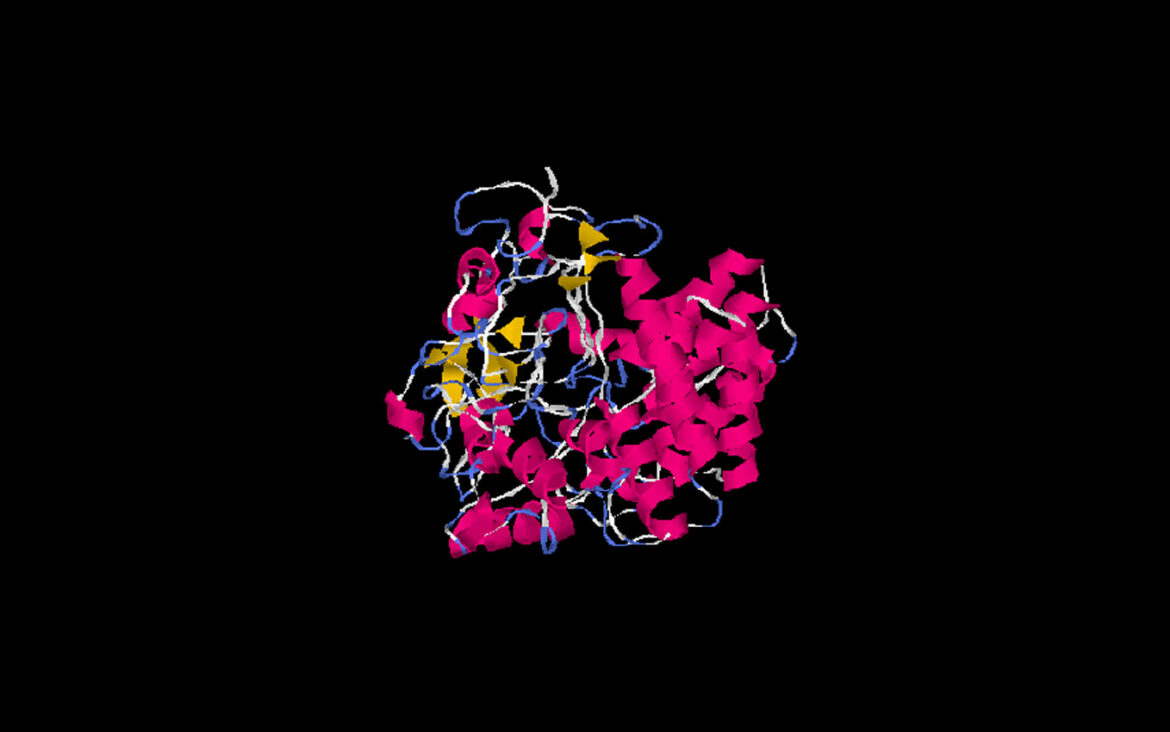
Slike su predviđeni 3-D oblici više od 200 miliona proteina, prikazani od strane sistema veštačke inteligencije pod nazivom AlphaFold. „Možete misliti da to pokriva ceo univerzum proteina“, rekao je Demis Hasabis na brifingu 26. jula. Hassabis je suosnivač i izvršni direktor DeepMind-a, kompanije sa sedištem u Londonu koja je kreirala sistem. Kombinujući nekoliko tehnika dubokog učenja, kompjuterski program je obučen da predvidi oblike proteina prepoznavanjem obrazaca u strukturama koji su već rešeni decenijama eksperimentalnog rada korišćenjem elektronskih mikroskopa i drugih metoda.
Prvo širenje veštačke inteligencije došlo je 2021. godine, sa predviđanjima za 350.000 proteinskih struktura – uključujući skoro sve poznate ljudske proteine. DeepMind se udružio sa Evropskim institutom za bioinformatiku Evropske laboratorije za molekularnu biologiju kako bi strukture učinio dostupnim u javnoj bazi podataka.
Masovno novo izdanje u julu proširilo je biblioteku na „skoro svaki organizam na planeti kome je sekvenciran genom“, rekao je Hassabis. „Možete da potražite 3-D strukturu proteina skoro isto tako lako kao i Google pretragu po ključnoj reči.
Ovo su predviđanja, a ne stvarne strukture. Ipak, istraživači su koristili neka od predviđanja za 2021. da bi razvili potencijalne nove vakcine protiv malarije, poboljšali razumevanje Parkinsonove bolesti, razradili kako da zaštite zdravlje pčela, stekli uvid u ljudsku evoluciju i još mnogo toga. DeepMind je takođe fokusirao AlphaFold na zanemarene tropske bolesti, uključujući Chagasovu bolest i lajšmanijazu, koje mogu biti iscrpljujuće ili smrtonosne ako se ne leče.
Mnogi naučnici su sa uzbuđenjem dočekali objavljivanje ogromnog skupa podataka. Ali drugi se brinu da će istraživači uzeti predviđene strukture kao prave oblike proteina. Još uvek postoje stvari koje AlphaFold ne može da uradi – i nije dizajniran da uradi – koje treba da se pozabave pre nego što proteinski kosmos u potpunosti dođe u fokus.
To što je novi katalog otvoren za sve je „ogromna korist“, kaže Džuli Forman-Kej, biofizičarka proteina u bolnici za bolesnu decu i Univerzitetu u Torontu. U mnogim slučajevima, AlphaFold i RoseTTAFold, drugi istraživači AI kojima su uzbuđeni, predviđaju oblike koji se dobro poklapaju sa profilima proteina iz eksperimenata. Ali, upozorava ona, „nije tako u potpunosti.“
Predviđanja su tačnija za neke proteine nego za druge. Pogrešna predviđanja mogu da navedu neke naučnike da pomisle da razumeju kako protein funkcioniše kada zaista ne razumeju. Mukotrpni eksperimenti ostaju ključni za razumevanje kako se proteini savijaju, kaže Forman-Kai. „Sada postoji osećaj da ljudi ne moraju da vrše eksperimentalno određivanje strukture, što nije tačno.“
Proteini počinju kao dugi lanci aminokiselina i savijaju se u mnoštvo kovrdžava i drugih 3-D oblika. Neki podsećaju na čvrste vadičep ringlets perm iz 1980-ih ili nabore harmonike. Drugi bi se mogli zameniti sa dečjim spiralnim škrabotinama.
Arhitektura proteina je više od samo estetike; može odrediti kako taj protein funkcioniše. Na primer, proteinima koji se nazivaju enzimi potreban je džep gde mogu da hvataju male molekule i izvode hemijske reakcije. A proteinima koji rade u proteinskom kompleksu, dva ili više proteina koji međusobno deluju kao delovi mašine, potrebni su pravi oblici da bi se formirali sa svojim partnerima.
Poznavanje nabora, namotaja i petlji oblika proteina može pomoći naučnicima da dešifruju kako, na primer, mutacija menja taj oblik da bi izazvala bolest. To znanje bi takođe moglo pomoći istraživačima da naprave bolje vakcine i lekove.
Godinama su naučnici bombardovali proteinske kristale rendgenskim zracima, fleš zamrznutim ćelijama i ispitivali ih pod snažnim elektronskim mikroskopom, i koristili druge metode da otkriju tajne oblika proteina. Takve eksperimentalne metode zahtevaju „mnogo vremena osoblja, mnogo truda i mnogo novca. Dakle, bilo je sporo“, kaže Tamir Gonen, membranski biofizičar i istraživač Medicinskog instituta Hauard Hjuz na Medicinskom fakultetu David Gefen na UCLA.