Da bi sprečili globalnu zdravstvenu krizu, naučnici širom sveta traže načine da se bore protiv bakterija koje mogu da izbegnu trenutni arsenal antibiotika.
Obećavajući cilj za nove i poboljšane antibiotike su ribosprekidači, mali delovi RNK koji regulišu proces neophodan za proizvodnju proteina od strane bakterijske ćelije. Ribosprekidači se nalaze skoro isključivo u bakterijama i mogu biti ciljani antibioticima tako da životinje ili ljudi nisu pogođeni. Sa potpunim razumevanjem kako funkcionišu ribosprekidači, istraživači bi mogli da razviju lekove koji ometaju ćelijsku mašineriju koja stvara potrebne proteine.
Sada su istraživači na Odeljenju za hemiju Univerziteta u Mičigenu i Institutu za prirodne nauke otkrili, koristeći kombinaciju biohemije, strukturne biologije i računarskog modeliranja, kako određeni riboprekidač reguliše sopstvenu sintezu.
Prvi korak u generisanju proteina iz genetskog koda naziva se transkripcija. Enzim RNK polimeraza (ili RNAP) putuje duž DNK, kopirajući genetske informacije koje se nalaze u DNK u lanac RNK. Tokom ovog procesa, RNAP će proći nekoliko „pauza“ dok čeka dalja uputstva iz ćelije. Mehanizmi za ovo pauziranje i ponovno pokretanje dugo su ostali nedostižni naučnicima, ali obećavaju da će postati savršena meta za antibiotike.
Tim, predvođen profesorom hemije Nilsom Valterom u saradnji sa laboratorijama profesorke LSI Melanie Ohi i bivšeg naučnika U-M Arona Franka, koristio je tehniku strukturne biologije nazvanu krioelektronska mikroskopija sa jednom česticom (krio-EM) da bi prvi put vizuelizovao kako nastaje ova transkripciona regulacija. Njihovi rezultati su objavljeni u Nature Structural & Molecular Biologi.
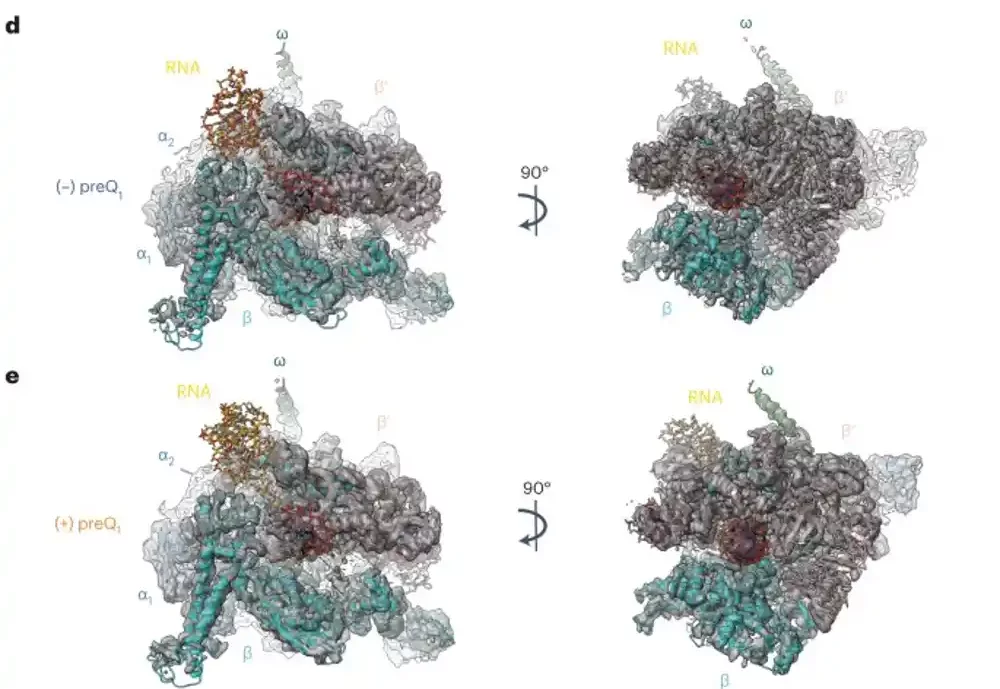
Volterova laboratorija je posmatrala određeni riboprekidač koji vezuje molekul koji proizvodi ćelija, nazvan preK 1 . Kada se molekul preK 1 veže za ribosprekidač, on menja oblik RNK, što onda omogućava da se RNAP ponovo nastavi duž DNK tako da se transkripcija nastavi.
Ribosprekidači su prvi put otkriveni 2002. godine, ali njihove specifične uloge vezane za mašineriju za transkripciju nisu dobro shvaćene. I nije teško shvatiti zašto je to tako, kaže Adrien Chauvier, naučnik iz Volterove laboratorije i stručnjak za riboprekidače.
„Ovo je situacija David protiv Golijata“, rekao je on. „RNAP je ovaj džinovski Golijat, a riboprekidač je David. Zbog ove drastične razlike u veličini, vizuelizacija gde i kako preK 1 reguliše transkripcionu pauzu jednako je pronalaženju igle u plastu sena.“
Ranija istraživanja iz Volterove laboratorije otkrila su da se pauza transkripcije uključuje i isključuje kao funkcija vezivanja preK 1 molekula za riboprekidač. Idući napred, Volterova laboratorija se udružila sa stručnjakom za krio-EM Ohijem da bi vizuelizovala šta se dešava.
„Ovaj rad je odličan primer snage bavljenja naukom na Univerzitetu u Mičigenu. Tri laboratorije sa različitim ekspertizom uspele su da oforme multidisciplinarnu saradnju koja je dovela do važnog i novog otkrića“, rekao je Ohi, takođe profesor ćelija i razvojna biologija na Medicinskom fakultetu U-M. „Ovi nalazi ne bi bili mogući bez ove sinergije, zajedno sa investicijama koje je univerzitet uložio u jačanje krio-EM i RNK biologije na U-M poslednjih godina.“
Krio-EM sa jednom česticom može odrediti strukture velikih proteinskih kompleksa izgradnjom 3D modela od miliona 2D slika čestica zamrznutih u različitim orijentacijama, otkrivajući strukture koje sadrže molekularne detalje koji pružaju funkcionalne uvide.
Strukturne informacije iz krio-EM sa jednom česticom su potvrdile ranija otkrića Volterove laboratorije, ali su takođe otkrile specifičnu promenu u obliku riboprekidača nikada ranije viđenu. Kada se preK 1 molekul veže, riboprekidač se okreće da komunicira sa RNAP-om da bi nastavio transkripciju.
Ova zapažanja su dodatno racionalizovana i potvrđena kroz saradnju sa Frankom, tada profesorom biofizike i hemije na Univerzitetu u Mičigenu i stručnjakom za računarsko modeliranje RNK. Sa detaljnim 3D modelima u ruci, tim za saradnju U-M sada ima preciznije razumevanje o tome kako ovaj ribosprekidač reguliše pauziranje transkripcije.
„Sada razumemo ceo proces regulacije ribosvitch-a i možemo da iskoristimo to znanje da posebno ciljamo ove kritične delove života bakterija, nadamo se da ćemo sprečiti nadolazeću krizu bakterija otpornih na više lekova“, rekao je Valter.