Ćelije raka creva imaju sposobnost da regulišu svoj rast pomoću genetskog prekidača za uključivanje i isključivanje kako bi maksimizirale svoje šanse za preživljavanje, fenomen koji su po prvi put primetili istraživači sa UCL i Univerzitetskog medicinskog centra Utreht.
Ranije se smatralo da je broj genetskih mutacija u ćeliji raka isključivo slučaj. Ali nova studija, objavljena u Nature Genetics, pružila je uvid u to kako se karcinom kreću kroz „čin evolucije balansiranja“.
Istraživači su otkrili da se mutacije u genima za popravku DNK mogu više puta stvarati i popravljati, delujući kao „genetski prekidači“ koji zaustavljaju rast tumora ili vraćaju kočnice, u zavisnosti od toga šta bi bilo najkorisnije za razvoj raka.
Istraživači kažu da bi se nalazi mogli potencijalno koristiti u personalizovanoj medicini raka kako bi se procenilo koliko je rak kod pojedinca agresivan kako bi im se mogao dati najefikasniji tretman.
Rak je genetska bolest uzrokovana mutacijama u našoj DNK. Oštećenje DNK se dešava tokom života, kako prirodno tako i zbog faktora životne sredine. Da bi se izborile sa ovim, ćelije su razvile strategije za zaštitu integriteta genetskog koda, ali ako se mutacije akumuliraju u ključnim genima povezanim sa rakom, tumori se mogu razviti.
Rak creva je četvrti najčešći rak u Velikoj Britaniji, sa oko 42.900 slučajeva godišnje. Iako je i dalje pretežno rak koji pogađa starije ljude, broj slučajeva među mlađim od 50 godina se povećava poslednjih decenija.
Poremećaj mehanizama popravke DNK je glavni uzrok povećanog rizika od raka. Oko 20% karcinoma creva, poznatih kao karcinomi sa nedostatkom popravke neslaganja (MMRd), uzrokovani su mutacijama u genima za popravku DNK. Ali ometanje ovih mehanizama popravke nije u potpunosti korisno za tumore. Iako dozvoljavaju razvoj tumora, svaka mutacija povećava rizik da će se imunološki sistem tela pokrenuti da napadne tumor.
Dr Marniks Jansen, viši autor studije sa UCL Instituta za rak i UCLH, rekao je: „Ćelije raka moraju da steknu određene mutacije da bi zaobišle mehanizme koji čuvaju naš genetski kod. Ali ako ćelija raka dobije previše mutacija, verovatnije je da privuče pažnju imunološkog sistema, jer se toliko razlikuje od normalne ćelije.
„Predvideli smo da bi razumevanje kako tumori iskorištavaju pogrešnu popravku DNK da bi pokrenuli rast tumora – dok istovremeno izbegavaju imunološku detekciju – moglo pomoći da se objasni zašto imuni sistem ponekad ne uspeva da kontroliše razvoj raka.“
U ovoj studiji, istraživači sa UCL analizirali su čitave sekvence genoma iz 217 MMRd uzoraka raka creva u bazi podataka 100.000 Genomes Project. Oni su tražili veze između ukupnog broja mutacija i genetskih promena u ključnim genima za popravku DNK.
Tim je identifikovao snažnu korelaciju između mutacija popravke DNK u genima MSH3 i MSH6 i ukupnog velikog obima mutacija.
Teorija da ove „flip-flop“ mutacije u genima za popravku DNK mogu kontrolisati stopu mutacije raka je zatim potvrđena u složenim modelima ćelija, nazvanim organoidi, uzgajanim u laboratoriji iz uzoraka tumora pacijenata.
Dr Suzanne van der Horst iz Univerzitetskog medicinskog centra Utreht rekla je: „Naša studija otkriva da mutacije popravke DNK u genima MSH3 i MSH6 deluju kao genetski prekidač koji kancer koristi da bi upravljao činom evolutivnog balansiranja.
„S jedne strane, ovi tumori bacaju kocku tako što isključuju popravku DNK kako bi izbegli odbrambene mehanizme tela. Iako ova neobuzdana stopa mutacije ubija mnoge ćelije raka, ona takođe proizvodi nekoliko ‘pobednika’ koji podstiču razvoj tumora.
„Zaista zanimljiv nalaz iz našeg istraživanja je ono što se dešava nakon toga. Čini se da rak ponovo uključuje prekidač za popravku DNK kako bi zaštitio delove genoma koji su i njima potrebni da prežive i da bi izbegao privlačenje pažnje imunog sistema. Ovo je prvi put kada smo videli mutaciju koja se može stvarati i popravljati iznova i iznova, dodavanjem ili brisanjem iz genetskog koda raka po potrebi.“
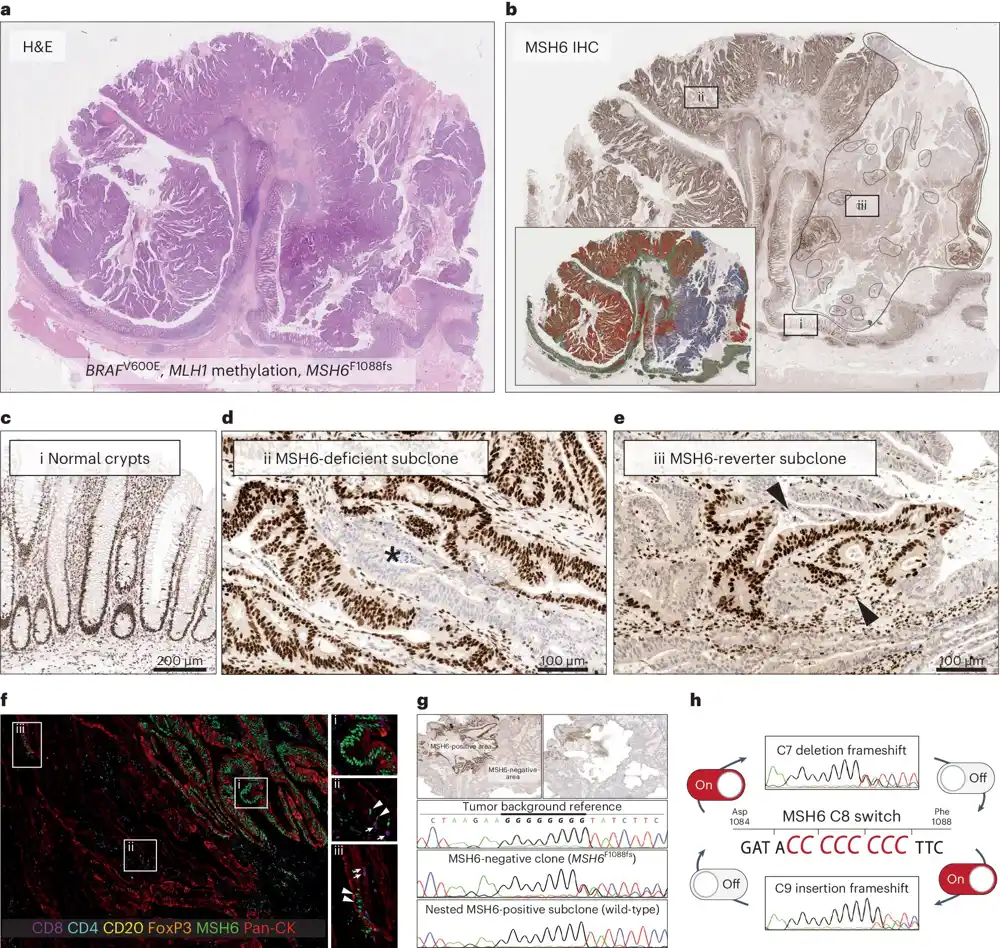
Dotične mutacije popravke DNK javljaju se u ponavljajućim delovima DNK koji se nalaze u ljudskom genomu, gde se jedno pojedinačno slovo DNK (A, T, C ili G) ponavlja mnogo puta. Ćelije često prave male greške u kopiranju u ovim ponavljajućim potezima tokom ćelijske deobe, kao što je promena osam Cs u sedam Cs, što remeti funkciju gena.
Dr Hamzeh Kaihanian, prvi autor studije sa Instituta za rak UCL i UCLH, rekao je: „Ranije se smatralo da je stepen genetskog poremećaja kod raka sveden isključivo na slučajnu akumulaciju mutacija tokom mnogo godina. Naš rad pokazuje da ćelije raka tajno prenameni ove repetitivne trakte u našoj DNK kao evolucione prekidače da fino podesi koliko se brzo mutacije akumuliraju u tumorskim ćelijama.
„Zanimljivo je da je ovaj evolucioni mehanizam ranije pronađen kao ključni pokretač otpornosti na tretman bakterija kod pacijenata lečenih antibioticima. Kao i ćelije raka, bakterije su razvile genetske prekidače koji povećavaju mutaciono gorivo kada je brza evolucija ključna, na primer kada se suoče sa antibioticima.
„Naš rad stoga dodatno naglašava sličnosti između evolucije drevnih bakterija i ljudskih tumorskih ćelija, glavne oblasti aktivnog istraživanja raka.“
Istraživači kažu da bi se ovo znanje potencijalno moglo koristiti za procenu karakteristika tumora pacijenta, što može zahtevati intenzivniji tretman ako je popravka DNK isključena i postoji potencijal da se tumor brže prilagodi kako bi izbegao lečenje – posebno na imunoterapije , koji su dizajnirani da ciljaju na jako mutirane tumore.
Nastavna studija je već u toku kako bi se otkrilo šta se dešava sa ovim prekidačima za popravku DNK kod pacijenata koji se leče od raka.
Dr Hugo Snippert, stariji autor studije sa Univerzitetskog medicinskog centra u Utrehtu, rekao je: „Sve u svemu, naše istraživanje pokazuje da je stopa mutacije prilagodljiva u tumorima i olakšava njihovu potragu za postizanjem optimalne evolucione sposobnosti. Novi lekovi bi mogli da onemoguće ovaj prekidač da podstakne efikasno imunološko prepoznavanje i, nadamo se, proizvede bolje rezultate lečenja za pogođene pacijente.“