Ćelije raka su kao gradovi u procvatu bez urbanističkih planera. Oni se brzo šire, a pritom nastali tumori troše više energije i drugih resursa nego što mogu dobiti iz obližnjih krvnih sudova.
Umesto da ograniče svoj rast na održivije stope, ćelije raka se prilagođavaju pronalazeći alternativne načine da pokupe ono što im je potrebno. Jedna strategija provlačenja koja preovladava kod duktalnog adenokarcinoma pankreasa (PDAC) uključuje ćelije raka koje preoblikuju svoje ćelijske površine kako bi uzele dodatne hranljive materije iz želeaste supstance između ćelija ili ekstracelularnog matriksa.
Ova ćelijska kontorzija je proces koji se naziva makropinocitoza. Pokazalo se da njegovo blokiranje i odsecanje energetskih i proteinskih gradivnih blokova koje obezbeđuje značajno suzbija rast tumora.
Dok su naučnici otkrili mnoge detalje o funkcionalnom značaju makropinocitoze u PDAC-u, ostaju mnoge misterije o tome kako PDAC ćelije kontrolišu svoju gimnastiku na površini ćelije kada se suoče sa nedostatkom adekvatnih hranljivih materija.
Istraživači iz NCI-ovog centra za rak u Sanford Burnham Prebisu objavili su nalaze 3. decembra 2024. u Nature Communications koji opisuju dva enzima koja su nedavno identifikovana zbog njihove uloge u regulisanju makropinocitoze.
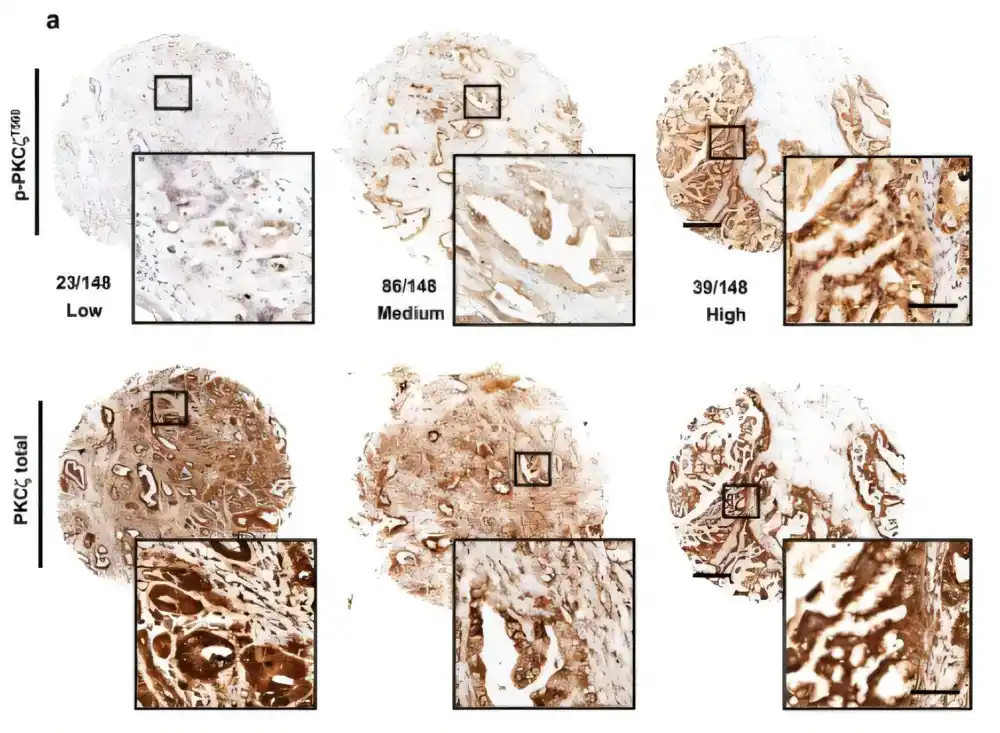
Cosimo Commisso, dr., stariji autor i privremeni direktor i zamenik direktora institutskog centra za rak, i saradnici su sproveli ispitivanje visokog protoka kako bi otkrili učešće atipične protein kinaze C (aPKC) zeta i jota.
„Mislili smo da kinaze verovatno igraju regulatornu ulogu pa smo pokrenuli ekran da uporedimo aktivnost 560 kinaza prisutnih kod ljudi dok su ćelije bile podvrgnute makropinocitozi u uslovima bez hranljivih materija“, rekao je Commisso.
Glutamin, jedna od 20 aminokiselina koje se koriste za izgradnju proteina u celom telu, bio je ključni hranljivi sastojak koji je zadržan jer se PDAC oslanja na glutamin mnogo više od drugih vrsta raka.
Sledeće pitanje sa kojim se suočio istraživački tim bilo je kako aPKC zeta i jota utiču na sposobnost PDAC ćelija da se hrane za alternativne izvore energije i aminokiselina. Normalno, aPKC enzimi su najpoznatiji po tome što pomažu u održavanju jedinstvenog oblika i strukture ćelija u različitim tkivima kako bi se olakšale njihove specijalizovane funkcije, poznate kao ćelijski polaritet.
„Polaritet ćelija je neophodan da bi se epitel koji okružuje naša tkiva i organe održao na veoma strukturiran i funkcionalan način“, rekao je dr Guillem Lambies Barjau, postdoktorski saradnik u laboratoriji Commisso i prvi autor studije.
„Rak, međutim, želi da se brzo proširi, pobegne iz tkiva porekla i napadne druga tkiva tako da izbegava strukturu polariteta ćelija kako bi rastao na nekontrolisan način.“
Naučnici su otkrili da su aPKC zeta i jota – i tri druga proteina sa kojima kinaze normalno stupaju u interakciju i vezuju se za regulisanje polariteta ćelija – prenamenjene od strane PDAC ćelija koje nemaju pristup glutaminu da bi povećale makropinocitozu i izvukle više alternativnih resursa iz svog okruženja.
U narednim eksperimentima, istraživački tim je testirao da li je ova prenamena aPKC zeta i jota u PDAC ćelijama doprinela rastu i opstanku ćelija raka.
„Oštećujući aPKC zeta ili jota u uslovima sa niskim nivoom glutamina koji oponašaju stanje PDAC tumora bez hranljivih materija u ljudskom telu, videli smo da PDAC ćelije nisu u stanju da se razmnožavaju bez ovih kinaza“, rekao je Commisso.
Istraživači su zatim pokušali da potvrde ove nalaze iz ćelijskih eksperimenata istražujući da li su se slični rezultati desili u mišjem modelu PDAC-a. Nakon eliminacije aPKC zeta ili jota kod mišjih PDAC tumora, miševi su doživeli značajno smanjenje rasta tumora u poređenju sa miševima sa tumorima koji su imali normalne nivoe aPKC.
„Takođe smo otkrili da je došlo do nižih nivoa makropinocitoze na mestima sa više hranljivih materija u jezgru tumora tretiranih da bi se uklonili aPKC“, rekao je Barjau.
„Zajedno, ovi rezultati u životinjskom modelu daju podršku našem opštem nalazu da aPKC zeta i jota doprinose kontroli makropinocitoze i da su potrebni za rast raka kao što je PDAC.“
U bacanju novog svetla na to kako karcinomi poput PDAC-a prevazilaze ograničene zalihe kako bi podstakli abnormalne stope rasta, naučnici su ukazali na potencijal za ciljanje aPKC-a za razvoj budućih tretmana raka.
„Ovaj rad naglašava kako ćelije raka pankreasa otimaju proteine polariteta ćelija da regulišu makropinocitozu i metabolizam tumora, i otkriva potencijalne terapijske ranjivosti“, rekao je Commisso.