Rezultati studije faze III koju je sproveo međunarodni tim istraživača otkrivaju da je mirikizumab efikasniji i da ima povoljan bezbednosni profil sa manje ozbiljnih neželjenih događaja u poređenju sa placebom za pojedince koji pate od umereno do teško aktivne Kronove bolesti.
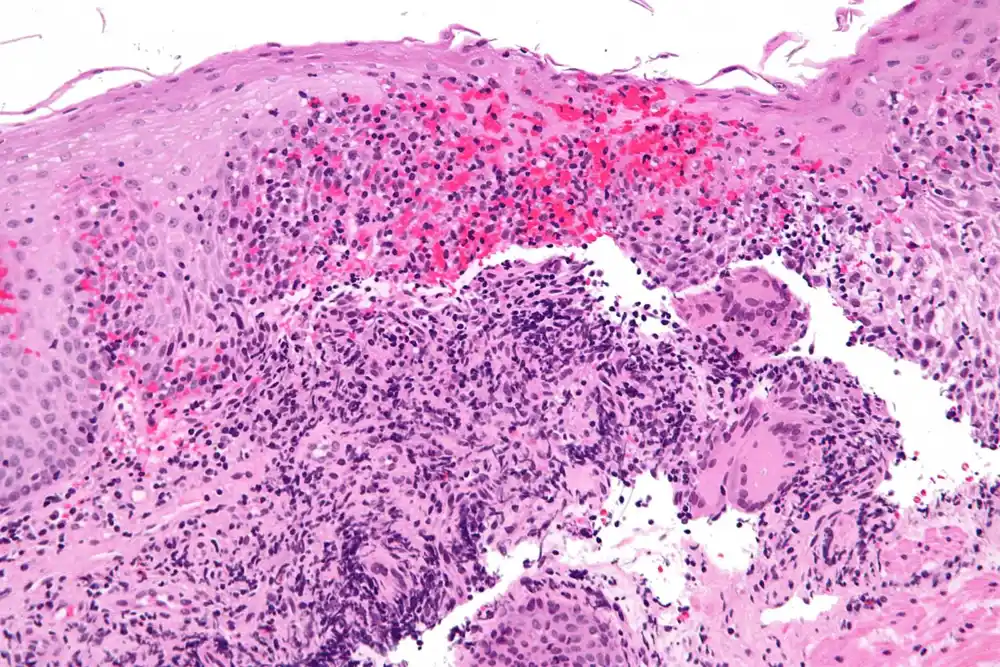
Kronova bolest je hronično, progresivno inflamatorno stanje creva koje karakteriše upala koja zahvata sve slojeve crevnog zida, što potencijalno dovodi do nepovratnog oštećenja creva i invaliditeta. Ovo može dovesti do nepovratnog oštećenja creva i invaliditeta.
Trenutni tretmani često ne uspevaju da postignu trajnu kontrolu simptoma i zarastanje sluzokože. Prethodne studije su identifikovale interleukin-23 kao kritičan citokin u patogenezi bolesti, što ga čini potencijalnom metom za nove terapijske intervencije.
U studiji, „Efikasnost i bezbednost mirikizumaba kod pacijenata sa umereno do teško aktivnom Kronovom bolešću: faza 3, multicentrična, randomizovana, dvostruko slepa, placebo kontrolisana i aktivno kontrolisana studija koja se leči,“ objavljeno na internetu u The Lancet, istraživači su upisali 1.150 odraslih pacijenata na 324 lokacije u 33 zemlje koji su pokazala netoleranciju ili neadekvatan odgovor na najmanje jednu odobrenu biološku ili konvencionalnu terapiju. Učesnici su nasumično raspoređeni da primaju mirikizumab, ustekinumab ili placebo.
Mirikizumab je konstruisano monoklonsko antitelo koje je već odobreno za lečenje ulceroznog kolitisa. Mirikizumab cilja i inhibira p19 podjedinicu interleukina-23 sa nizvodnim efektom za koji se istraživači nadaju da će utišati put upale povezane sa Kronovom bolešću.
Koprimarne krajnje tačke procenjivale su superiornost mirikizumaba nad placebom procenom kliničkog odgovora koji je prijavio pacijent u 12. nedelji u kombinaciji sa endoskopskim odgovorom ili kliničkom remisijom pomoću indeksa aktivnosti Crohnove bolesti (CDAI) u 52. nedelji.
Rezultati su otkrili da je 38,0% pacijenata koji su primali mirikizumab postiglo kombinovanu krajnju tačku kliničkog odgovora u 12. nedelji i endoskopskog odgovora u 52. nedelji, u poređenju sa 9,0% u placebo grupi. Pored toga, 45,4% grupe koja je primala mirikizumab je postigla kliničku remisiju od strane CDAI u 52. nedelji u odnosu na 19,6% za placebo.
U poređenju sa ustekinumabom u postizanju kliničke remisije u 52. nedelji, 54,1% pacijenata sa mirikizumabom je postiglo remisiju u poređenju sa 48,4% za ustekinumab. U endoskopskom odgovoru u 52. nedelji, 48,4% pacijenata sa mirikizumabom naspram 46,3% pacijenata sa ustekinumabom ispunilo je ovu krajnju tačku.
Incidenca neželjenih događaja i prekida terapije bili su niži u grupi koja je primala mirikizumab u poređenju sa placebom. Ozbiljni neželjeni događaji su se javili kod 10,3% pacijenata na mirikizumabu, 10,7% na ustekinumabu i 17,1% na placebu. Bezbednosni profil mirikizumaba bio je u skladu sa prethodnim nalazima, što ukazuje na povoljan odnos koristi i rizika za njegovu upotrebu u lečenju aktivne Kronove bolesti.
Rezultati ispitivanja pokazuju da mirikizumab može da odgovori na nezadovoljene medicinske potrebe pružanjem trajnijih i efikasnijih opcija lečenja. Sposobnost mirikizumaba da održi kliničku remisiju i smanji zapaljenje tokom 52 nedelje je veoma ohrabrujuća zbog njegove potencijalne uloge u poboljšanju kvaliteta života osoba koje se bore sa Kronovom bolešću.