Svako ko želi da proizvodi lekove, plastiku ili đubrivo korišćenjem konvencionalnih metoda potrebna je toplota za hemijske reakcije – ali nije tako sa fotohemijom, gde svetlost daje energiju. Proces za postizanje željenog proizvoda takođe često zahteva manje međukoraka.
Istraživači sa Univerziteta u Bazelu sada idu korak dalje i pokazuju kako se energetska efikasnost fotohemijskih reakcija može povećati 10 puta. Održivije i isplativije aplikacije su sada zapanjujuće blizu.
Industrijske hemijske reakcije se obično odvijaju u nekoliko faza u različitim privremenim proizvodima. Fotohemija omogućava prečice, što znači da je potrebno manje srednjih koraka. Fotohemija vam takođe omogućava da radite sa manje opasnim supstancama nego u konvencionalnoj hemiji, jer svetlost proizvodi reakciju u supstancama koje ne reaguju dobro pod toplotom. Međutim, do ove tačke nije bilo mnogo industrijskih primena za fotohemiju, delom zato što je snabdevanje energijom svetlošću često neefikasno ili stvara neželjene nusproizvode.
Istraživačka grupa koju vodi profesor Oliver Venger sa Univerziteta u Bazelu sada opisuje fundamentalni princip koji ima neočekivano snažan uticaj na energetsku efikasnost fotohemije i može povećati brzinu fotohemijskih reakcija. Njihovi rezultati su objavljeni u Nature Chemistry.
U slučaju ovakve reakcije, početni molekuli su u tečnom rastvoru. Ako primaju energiju u obliku svetlosti, mogu da razmenjuju elektrone jedni sa drugima i formiraju radikale. Ovi izuzetno reaktivni molekuli se uvek javljaju u parovima i ostaju okruženi rastvaračem, koji zatvara parove radikala kao neka vrsta kaveza.
Da bi radikali mogli da nastave da reaguju na željene ciljne proizvode, potrebno je da „izbiju“ iz ovog kaveza i van njega pronađu partnera za reakciju. Tim koji okružuje Vengera i njegovog postdoktora dr Cui Vanga identifikovao je ovaj proces izbijanja kao odlučujući korak koji ograničava energetsku efikasnost i brzinu fotohemijskih reakcija.
Sve dok radikali ostaju u parovima u kavezu sa rastvaračem, oni mogu spontano da reaguju jedan sa drugim nazad u početne materijale. Ova obrnuta reakcija troši energiju jer koristi samo već apsorbovanu svetlost da se vrati na početnu tačku.
Tim iz Bazela uspeo je da uspori ovu obrnutu reakciju i samim tim da radikalima više vremena da napuste kavez. Što je neželjena obrnuta reakcija bila duža, to je više radikala bilo u stanju da izbije i energetski efikasniji i brži su se razvijali željeni ciljni proizvodi.
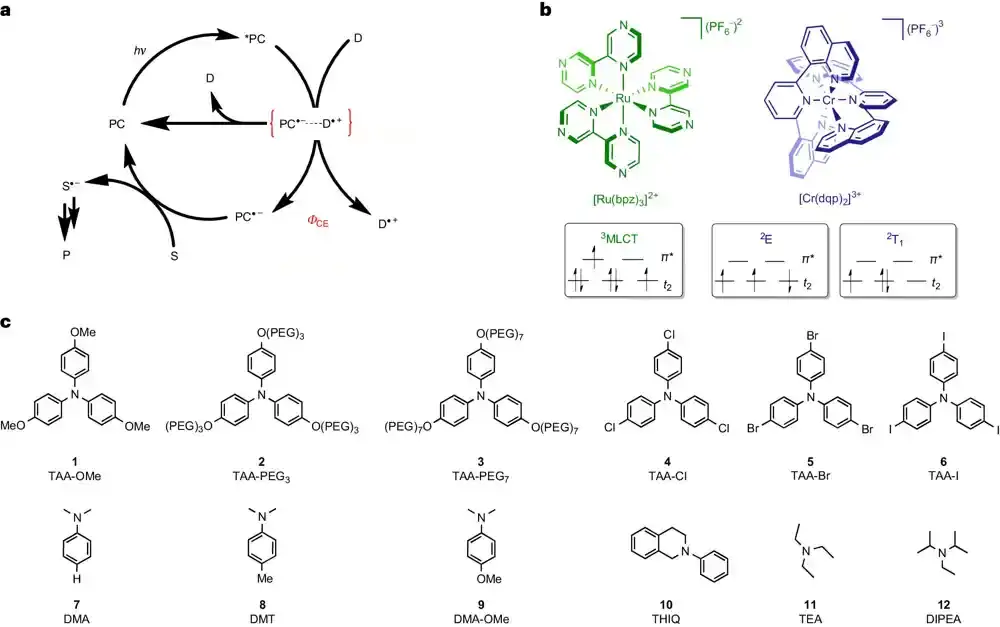
Vang, koja sada ima poziciju docenta na Univerzitetu u Osnabruku, koristila je dve posebne boje u svojoj studiji, od kojih obe apsorbuju svetlost i skladište njenu energiju na kratak period pre nego što je koriste za formiranje parova radikala. Međutim, jedna od dve ispitivane boje bila je u stanju da uskladišti znatno više energije od druge i prenese je na radikale.
Zbog dodatne energije, radikali su uspeli da napuste kavez sa rastvaračem i do deset puta efikasnije. Shodno tome, ciljni proizvodi se proizvode sa do deset puta većom energetskom efikasnošću. „Ova direktna veza između radikala koji izlaze iz kaveza sa rastvaračem i efikasnog formiranja ciljnih proizvoda je zapanjujuće jasna“, rekao je Vang.
Ključni nalaz je da određene boje mogu osloboditi više radikala od drugih po količini apsorbovane svetlosti. „Izbor boje se može koristiti za povećanje energetske efikasnosti fotohemijskih reakcija“, rekao je Venger. Zauzvrat, on navodi da je energetska efikasnost takođe odlučujući kriterijum za industrijsku upotrebu fotohemije.