Super hlađenjem molekula na površini moždanih ćelija na oko minus 180 stepeni Celzijusa – skoro dvostruko hladnijim od najhladnijih mesta na Antarktiku – naučnici iz Johns Hopkins Medicine kažu da su utvrdili kako široko korišćeni lek za epilepsiju deluje da ublaži ekscitabilnost moždanih ćelija i pomažu u kontroli, mada ne i izlečenju, napadima.
Istraživanje, objavljeno 4. juna u Nature Structural & Molecular Biology, identifikuje kritične veze između aktivnosti leka za epilepsiju perampanela i rezultujućih pokreta AMPA receptora — površinskog molekula moždane ćelije. Istraživači kažu da bi otkrića na kraju mogla da pomognu u dizajniranju novih lekova koji ciljaju na receptor za lečenje drugih neuroloških stanja kao što su Alchajmerova bolest, šizofrenija, smetnje u učenju, karcinom mozga koji se naziva glioblastom i hronični bol.
AMPA receptor igra kritičnu ulogu za jedan od najzastupljenijih neurotransmitera u mozgu — glutamat — koji aktivira moždane ćelije (neurone) povezujući se sa proteinom na površini ćelije (AMPA) u vezi nalik na Pac-man, u kojoj AMPA receptori progutati glutamat.
Do četiri molekula glutamata mogu se vezati za jedan AMPA receptor. Veza omogućava poplavi jona (pozitivno naelektrisanih čestica) da uđu u neuron i aktiviraju ga (uzbude).
„AMPA receptori i glutamat su neophodni za većinu aspekata života, uključujući procese učenja, pamćenja i kodiranja iskustava“, kaže dr Edvard Tvomi, docent za biofiziku i biofizičku hemiju na Medicinskom fakultetu Univerziteta Džon Hopkins. „Većina neuroloških bolesti se na neki način vraća do AMPA receptora i glutamata.“
Tvomijeju se obratio neuronaučnik Richard Huganir, dr., koji proučava AMPA receptore već 40 godina, da sarađuje na istraživanju kako bi bolje razumeo strukturu receptora i njihov proces vezivanja glutamata.
Poznato je da prekomerna aktivacija (ekscitacija) AMPA receptora izaziva epilepsiju. Perampanel, koji cilja na AMPA receptor, jedini je lek koji je odobrila američka Uprava za hranu i lekove da cilja AMPA receptore, ali mnoge farmaceutske kompanije rade na sličnim jedinjenjima, kažu istraživači.
„Ovaj lek je prvobitno otkriven 1980-ih, a njegov precizan mehanizam je dugotrajna misterija“, kaže Tvomi.
„Znamo da ovaj lek ne blokira i ne zaglavi se u jonskim kanalima receptora“, kaže Huganir, ugledni profesor neuronauke i psiholoških nauka i nauke o mozgu Bloomberg i direktor Odeljenja za neuronauku Solomona H. Snajdera. Drugi naučnici su otkrili gde se perampanel vezuje za AMPA receptore u džepovima oko jonskog kanala, ali nisu pronašli način na koji ta veza remeti protok jona.
Da bi proučili mehanizam, istraživači su se okrenuli krio-elektronskoj mikroskopiji (crioEM), koja je evoluirala u poslednje dve decenije kao moćno sredstvo za proučavanje struktura milion puta manjih od širine ljudske kose.
Johns Hopkins postdoktorski saradnik V. Dilan Hale, Ph.D., koji radi u laboratorijama Tvomei i Huganir, izveo je većinu eksperimenata i analiza u Beckman centru za CrioEM u Johns Hopkinsu, gdje su super hladili biološke molekule i snimali različite vremenske tačke.
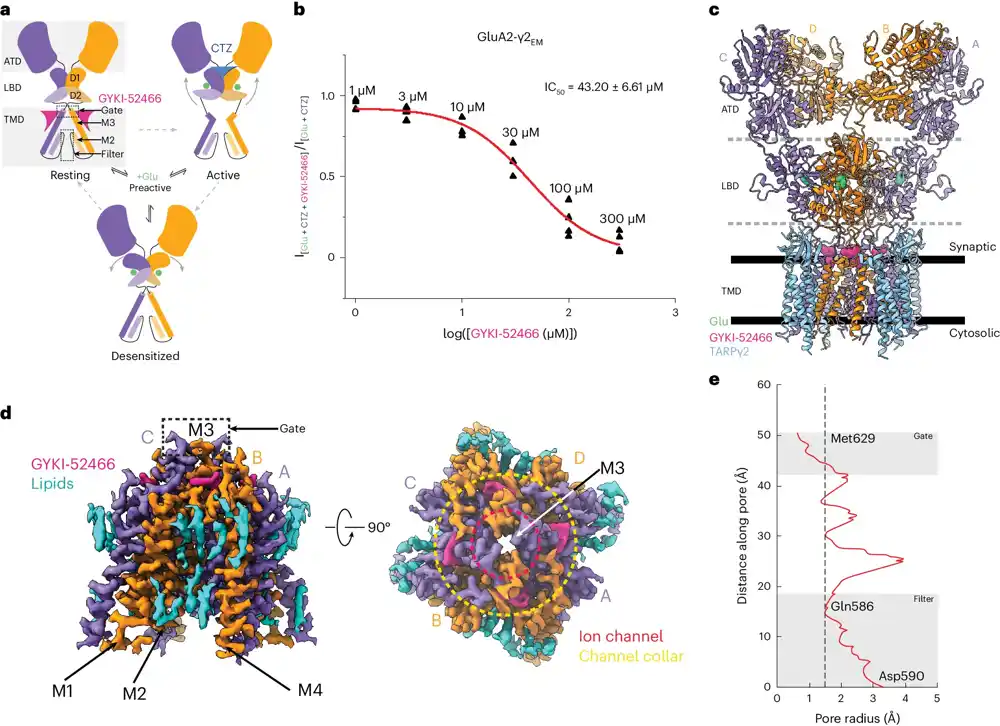
Za ovu studiju, istraživači su analizirali milione slika AMPA receptora u moždanim ćelijama sa modela miševa i pacova i njihovu interakciju sa prvobitno otkrivenom verzijom perampanel leka, GIKI-52466. „Ove interakcije se dešavaju na super maloj skali, oko 1 do 2 angstrema“, kaže Tvomi.
Oni su pogledali vezivanje leka GIKI-52466, sa i bez glutamata. Takođe su izvršili električne snimke jonskog toka i fiziološke studije na miševima kako bi upotpunili crioEM slike.
Naučnici su koristili veštačku inteligenciju i alate za mašinsko učenje da usredsrede i kombinuju crioEM slike u 3D rekonstrukciju receptora.
Kada se glutamat veže za AMPA receptor u jednom od četiri položaja, lanac receptora se spušta i otvara jonski kanal omogućavajući protok jona, slično tome kako vučni lanac oslobađa vodu iz glave tuša.
Istraživači su otkrili da su dve od četiri pozicije vezivanja glutamata najvažnije u sposobnosti leka GIKI-52466 da blokira protok jona.
„Lek se vezuje za AMPA receptor i sprečava otvaranje jonskog kanala blokiranjem sposobnosti glutamata da povuče lanac koji otvara jonski kanal“, kaže Tvomi. „Izgleda da razdvaja regione koji vezuju glutamat jedan od drugog i dovodi receptor u desenzibilizovano stanje.“
Huganir takođe planira da sarađuje sa Tvomijem kako bi koristio crioEM za proučavanje šta se dešava sa AMPA receptorom kada je mutiran.
„Želimo da znamo šta nije u redu sa strukturom receptora koja onemogućava njegovu funkciju“, kaže Huganir. „U teoriji, mogli bismo razviti lekove koji bi receptor učinili aktivnijim za lečenje stanja u kojima je struktura receptora promenjena.“