Genetski planovi unutar naše DNK se funkcionalno ostvaruju kroz proteine, koji su u osnovi strukture i aktivnosti našeg tela. Ipak, proteom – svi proteini unutar ćelije ili datog područja – ostaje relativno misteriozan jer su proteinski pejzaži neverovatno složeni. Ljudi, na primer, prave desetine hiljada različitih proteina.
Da bi pomogao u dešifrovanju ove složenosti, tim istraživača sa Univerziteta Stanford predvodio je razvoj nove metode, nazvane TransitID, za praćenje kompletne aktivnosti proteina u živim ćelijama. Ovaj metod je detaljno opisan u radu objavljenom 28. juna u časopisu Cell.
Postojeće tehnike za ovaj zadatak, mikroskopija i proteomija masene spektrometrije, ili omogućavaju naučnicima da proučavaju samo nekoliko proteina istovremeno u živoj ćeliji, ili daju veoma detaljan, ali ipak, snimak svih proteina u mrtvoj ćeliji.
„Naša nova tehnika vam omogućava da kombinujete prednosti i mikroskopije i proteomike masene spektrometrije tako što ćete zapravo posmatrati žive uzorke – uključujući njihovu dinamiku dok se kreću i funkcionišu – i videti na nepristrasan način sve proteine odjednom“, rekla je Alis Ting , profesor genetike na Stanfordskoj medicini i biologije na Fakultetu humanističkih nauka i nauka, koji je viši autor rada. „Nije bilo metoda koje su kombinovale te snage ranije.“
TransitID takođe radi na proteinima koji se kreću između ćelija. Praćenje proteina na ovom nivou detalja i živahnosti moglo bi otkriti neispričane informacije o tome kako ćelije komuniciraju. Pored toga, postoje očigledne aplikacije za istraživanje različitih bolesti i tretmana, uključujući i oblasti raka i neurodegenerativnih bolesti.
„Uzbudljivo je da postoje tako široke aplikacije za ovo“, rekla je Joleen Cheah, dr. kandidat na Stanfordu i ko-vodeći autor rada. „Već smo primili mnogo upita o TransitID-u i uspostavili mnoge saradnje sa drugim laboratorijama koje su zainteresovane da ga koriste.“
Vrlo jednostavno rečeno, TransitID prati sve proteine na određenom putu označavajući sve molekule unutar određenog radijusa odabranih početnih i krajnjih lokacija. Prvo, dva enzima koje je prethodno razvila Ting laboratorija, nazvana TurboID i APEKS, postavljaju se na svaki kraj putovanja. Kada su istraživači spremni da počnu sa praćenjem proteina, uvode biotin vitamina B, koji uzrokuje da TurboID prska biotin na sve okolne molekule – uključujući proteine – označavajući ih.
Istraživači zatim isperu ćeliju od viška biotina i dopuštaju joj da obavlja svoju uobičajenu aktivnost. Kada misle da su proteini imali dovoljno vremena da putuju, onda dodaju hemijsko jedinjenje alkin-fenol, koje izaziva isto dejstvo prskanja na APEKS kraju.
Istraživači tumače pojedinačne izlete proteina koji su se kretali između označenih lokacija razbijanjem ćelijske membrane i analizom sadržaja. Neki proteini se nikada neće pomeriti, bilo da imaju samo TurboID oznake ili samo APEKS oznake. Oni koji imaju oboje, putovali su između. A sve što nije bilo obeleženo nalazilo se izvan putovanja koje vas zanima.
Da bi testirali svoj alat, istraživači su prvo sproveli dva eksperimenta sa detaljima o poznatoj aktivnosti proteina. Oni su pratili proteine koji su se kretali između tečnosti citoplazme (citosola) do mitohondrija, koji postoje za razliku od proteina koji su proizvod mitohondrijalne DNK i stoga potiču iz mitohondrija.
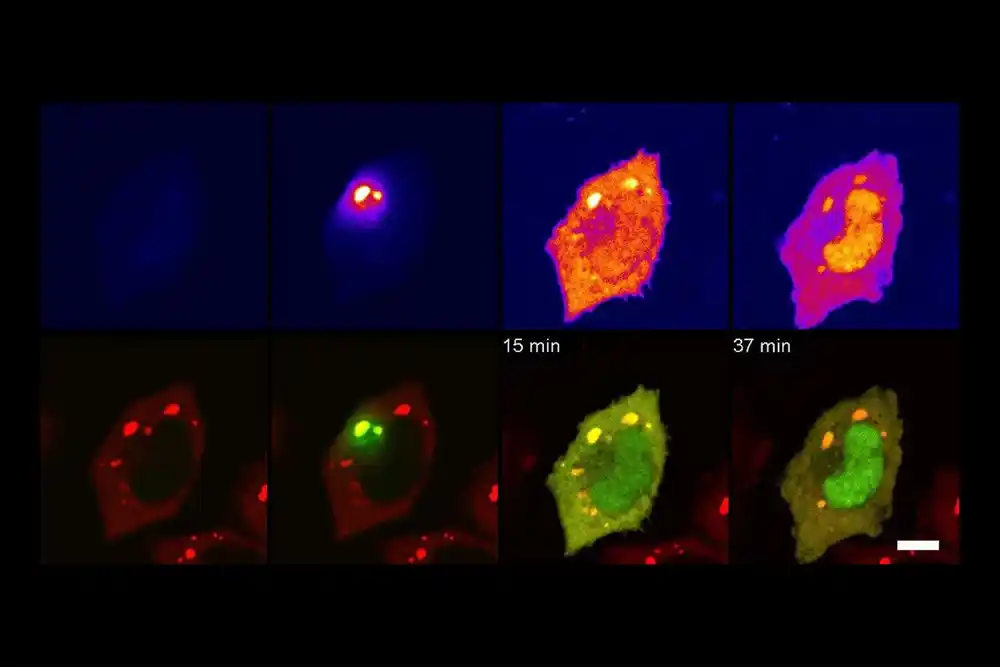
U sledećem eksperimentu, istraživači su pratili kako se kretanje proteina iz citosola u jezgro menja kada se ćelija podvrgne oksidativnom stresu. Rezultati oba ova eksperimenta su se pokazali kao što se očekivalo, što je značilo da je TransitID uspešno radio.
Zatim su istraživači koristili svoju tehniku da istraže promet proteina u delove ćelije koji nisu vezani membranama – konkretno, granule stresa, koje su kondenzacije proteina i RNK koje se formiraju kao odgovor na ćelijski stres.
„Biomolekularni kondenzati, kao što su granule stresa, su veoma dinamične strukture koje brzo i kontinuirano razmenjuju sastojke sa srodnim strukturama. TransitID nam omogućava po prvi put da pratimo sudbinu ovih sastojaka“, rekao je J. Paul Tailor, naučni direktor i izvršni potpredsednik predsednik Dečje istraživačke bolnice St. Jude, koji je koautor rada.
Rezultati ovog eksperimenta bili su iznenađujući. Dok su istraživači analizirali proteom granula stresa, otkrili su JUN, dobro poznati faktor transkripcije koji je pojačano/previše eksprimiran kod više vrsta raka.
„Niko ga nikada ranije nije pronašao u granulama stresa“, rekla je Ting. „Dakle, kada smo ga tamo našli, skoro da mu nismo verovali.
Nakon što su potvrdili njegovo prisustvo, istraživači su dalje istraživali i utvrdili da je JUN izgledao u granulama stresa kao zaštitni mehanizam. Otkrili su da se, pod oksidativnim stresom, JUN premešta u granule stresa kako bi izbegao svoj alternativni odgovor na stres – agregiranje i zatim odlaganje kao nepoželjan agregirani nered – što održava JUN zdravim i dostupnim da nastavi sa radom kada stres prođe.
Poslednji eksperiment sa TransitID-om koji je uključen u ovaj rad pratio je aktivnost proteina između makrofaga i ćelija raka, koja postoji u notorno složenom i bučnom proteinskom okruženju.
Sa hiljadama zahteva za TurboID i APEKS koji su već primljeni od laboratorija širom sveta kao odgovor na prethodni rad, istraživači znaju da će njihovo novo shvatanje ovih postojećih favorita omogućiti uzbudljive rezultate kako u temeljnoj tako i u primenjenoj nauci.
„Očekujem da će širok spektar naučnika brzo usvojiti ovaj pristup, slično drugim inovativnim tehnikama razvijenim u Alisinoj laboratoriji“, rekao je Tejlor. „Ovaj alat je posebno važan proboj koji omogućava istraživanje kondenzata jer su to veoma dinamične strukture.“
„Uzbuđen sam zbog jednostavnosti metode i koliko je ona dostupna, s obzirom na ono što već postoji“, rekla je Ting. „Koristi komercijalno dostupne reagense i ljudi ne moraju da rade nikakvu organsku hemiju u sopstvenim laboratorijama da bi koristili metod, a ipak mogu pristupiti potpuno novoj biologiji koja ranije nije bila vidljiva.“
Tim još uvek vidi prostor za poboljšanje, posebno sa ciljem da optimizuje svoj proces i oslanja se na manje toksične hemikalije. Za sada, TransitID je ograničen na upotrebu u ćelijskim kulturama, ali bi se, uz nežnije hemikalije, mogao koristiti za praćenje detaljne dinamike proteina kod živih životinja.