Zdrave ćelije naporno rade na održavanju integriteta naše DNK, ali povremeno se hromozom može odvojiti od ostalih i raspasti tokom ćelijske deobe. Sićušni fragmenti DNK se zatim ponovo sastavljaju nasumičnim redosledom u novoj ćeliji, ponekad stvarajući mutacije gena raka.
Ovo hromozomsko razbijanje i preuređenje naziva se „hromotripsis“ i javlja se kod većine ljudskih karcinoma, posebno kod karcinoma kostiju, mozga i masnog tkiva. Hromotripsa je prvi put opisana pre nešto više od decenije, ali naučnici nisu razumeli kako su plutajući delovi DNK mogli da se ponovo spoje.
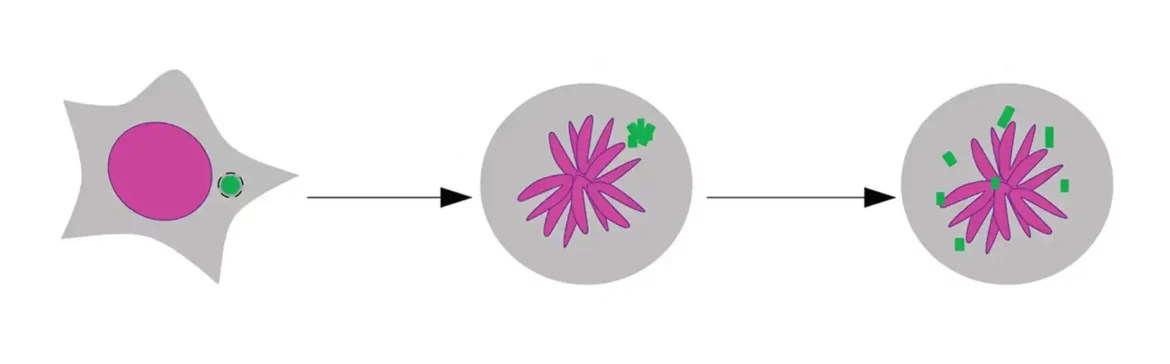
U studiji objavljenoj u Nature, istraživači sa Univerziteta Kalifornije u San Dijegu odgovorili su na ovo pitanje, otkrivajući da su razbijeni fragmenti DNK zapravo povezani zajedno. Ovo im omogućava da putuju kao jedno tokom ćelijske deobe i da budu ponovo inkapsulirani u jednoj od novih ćerki ćelija, gde se ponovo sklapaju drugačijim redosledom.
„Slično je razbijenom šoferšajbnu automobila, gde je sigurnosno staklo dizajnirano da zadrži sve polomljene delove na mestu“, rekao je viši autor studije Don V. Klivlend, dr, uvaženi profesor i predsedavajući Odeljenja za mobilne i Molekularna medicina na UC San Diego School of Medicine. „Ovde smo pronašli sigurnosno staklo i identifikovali nekoliko njegovih osnovnih komponenti, koje sada možemo istražiti kao terapeutske mete.
Kada se hromozomi pokvare i preurede, to može pokrenuti ili pogoršati rak na nekoliko načina. Na primer, ako je gen supresor tumora slomljen u procesu, ćelija će postati ranjivija na formiranje tumora.
U drugim slučajevima, geni koji obično nisu blizu jedan drugom na hromozomu mogu se iznenada spojiti da bi se proizveo novi onkogeni fuzioni protein. Tokom hromotripse, mnoge takve promene se dešavaju istovremeno, a ne postepeno, čime se ubrzava razvoj raka ili njegova otpornost na terapiju.
Sada kada su istraživači identifikovali rani korak u ovom procesu – vezivanje razbijenih fragmenata DNK – pitali su se da li mogu da ga zaustave. Uništavanjem vezice, oni mogu sprečiti formiranje preuređenih hromozoma, čime se smanjuje broj ćelija koje potencijalno nose kancerogene mutacije.
Da bi to uradio, postdoktorski saradnik i prvi autor studije Prasad Trivedi, dr., konstruisao je modifikovanu verziju jednog od proteina tethera tako da je mogao da izazove njegovo uništenje na zahtev. Kada je to uradio, veza se raspala, fragmenti DNK se nisu skupili i rezultirajuće ćelije su pokazale smanjeno preživljavanje.
Autori sugerišu da proteini u ovom tether kompleksu, posebno ćelijski inhibitor PP2A (CIP2A), sada mogu biti atraktivna terapeutska meta za hromozomski nestabilne tumore.
„Proces nege i popravke hromozoma doprinosi raku na mnogo načina, tako da što više razumemo kako funkcioniše, to bolje možemo da ga fino podesimo za lečenje raka“, rekao je Klivlend.