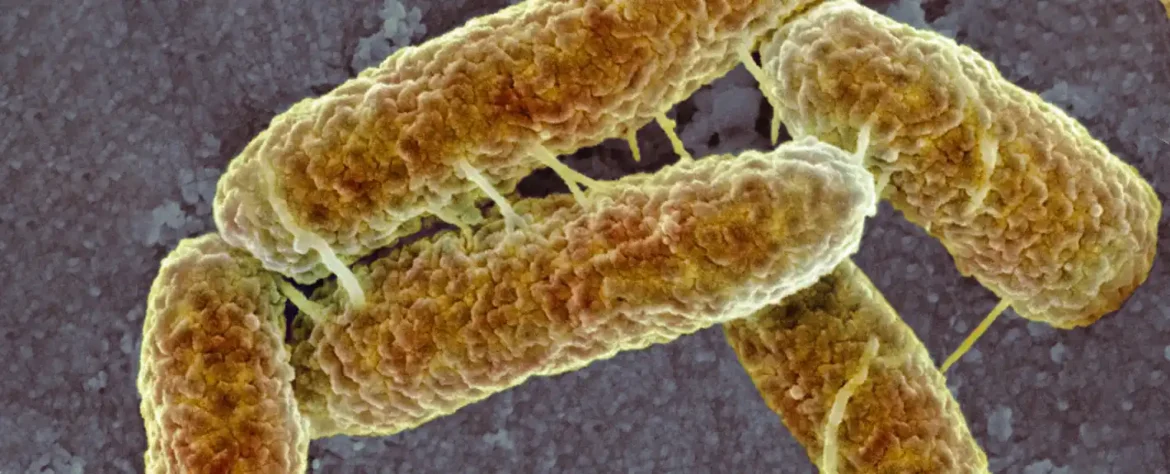
Bakterije mogu razviti povećanu novu osetljivost na nivoe kiseline kada su izložene različitim ekstremima životne sredine u laboratoriji, pokazuje nova studija.
Ovo čulo pokreće kaskadu različitih ekspresija gena, omogućavajući mikrobima da se rekonfigurišu prema ekstremima koji se stalno menjaju.
Od najmanjih ćelija do najvećih kitova, ceo život se suočava sa izazovom stalno promenljivih i biciklističkih uslova životne sredine.
Da bismo bolje razumeli kako se možemo fiziološki savijati do takvih ekstrema, mikrobiolog Sara Vortan sa Univerziteta Vanderbilt u Nešvilu i njen tim gurnuli su bakteriju Escherichia coli do krajnosti.
Neke od populacija bakterija bile su u stanju da brzo evoluiraju genetske mutacije koje su im pomogle da napreduju. Rakovi takođe koriste nastale mutacije kako bi stvorili sebi povoljnije okruženje.
„Naši rezultati sugerišu da [ove mutacije] mogu poslužiti za brzu koordinaciju složenih fizioloških odgovora putem pH sensinga i rasvetljavanja načina na koji ćelijske populacije koriste znakove životne sredine za koordinaciju brzih odgovora na složena, fluktuirajuća okruženja“, pišu istraživači u svom radu.
Vortan i njegove kolege su kreirali svoju intenzivnu eksperimentalnu verziju promena u životnoj sredini izlažući 16 populacija E. coli napadima ekstremne, dugotrajne gladi pre nego što su ih prebacili u sveže okruženje bogato hranljivim materijama i ponovili proces.
Kako su mikrobi gladovali, metabolički otpad se akumulirao, uzrokujući drastične promene u pH vrednosti životne sredine. Bakterije su tada dobile novi početak sa novim resursima svakih 100 dana, replicirajući ciklus gozbe i gladi sa kojima se život često suočava u stvarnom svetu.
Jedna promena proteinskog gradivnog bloka pojavila se i proširila u sedam populacija bakterija, uglavnom unutar samo prvih 300 dana eksperimenta. Ova promena aminokiselina iz arginina u histidin dogodila se u Rho proteinu – molekulu koji je uključen u govorenje mašineriji za proizvodnju proteina bakterije kada da prestane sa proizvodnjom.
„Ova mutacija u rhou se više puta javljala u našim laboratorijskim evolucijskim kulturama“, objašnjava mikrobiolog sa Univerziteta Vanderbilt Megan Behringer.
„Vratili smo se našim genomskim podacima i primetili da se svaka mutacija u rho javlja zajedno sa mutacijom u genu pod nazivom ‘idcI’. Ne zna se mnogo o ovom genu, ali nedavne studije sugerišu da on može imati ulogu u pH homeostazi.“
Normalni Rho protein pomaže ćelijama bakterija da se bolje ponašaju u stanju gozbe, ali predstavlja smetnju kada se njegov vlasnik suoči sa glađu. Vortan i tim su otkrili da mutirani idcI omogućava ćelijama da bolje tolerišu promene u Rho proteinu.
Čini se da mutacija idcI reaguje na promene pH. Dakle, deluje kao prekidač koji se uključuje promenama u okruženju da bi pokrenuo promene unutar pojedinačnih ćelija.
„Iako bakterije međusobno komuniciraju kroz svoje vanćelijsko okruženje, pojedinačne ćelije imaju određenu kontrolu nad svojim intracelularnim okruženjem“, kaže Braton.
Ovi geni rade zajedno kako bi omogućili ćelijama da se lakše fiziološki savijaju prema uslovima sredine koja se stalno menja. Tim je pronašao nekoliko primera istog mehanizma u prirodi.
„Pronašli smo ga u ovom zanemarenom patogenu, Bartonella bacilliformis, koji uzrokuje Carrionovu bolest u Andskim dolinama Južne Amerike“, kaže Behringer.
„Ova vrsta bakterija je već bila poznata po pH osećaju jer se mora brzo prilagoditi od creva insekata sa visokim pH na neutralni pH ljudske krvi kada se prenosi putem vektora peščane mušice.
Biti dobar u ovakvom prilagođavanju pomaže ćelijama da nadmaše druge, kao što vidimo kod raka. Čini se da rakovi koriste sličan mehanizam da povećaju i svoj unutrašnji pH, stvarajući kaskadu različitih ekspresija gena koji se zatim koriste za preoblikovanje ćelijskog okruženja oko sebe.
Ovi rezultati ilustruju „moć eksperimentalne evolucije za identifikaciju funkcionalno važnih mutacija relevantnih za prirodna okruženja“, zaključuju Vortan i tim.
Ovo istraživanje je objavljeno u PNAS-u.