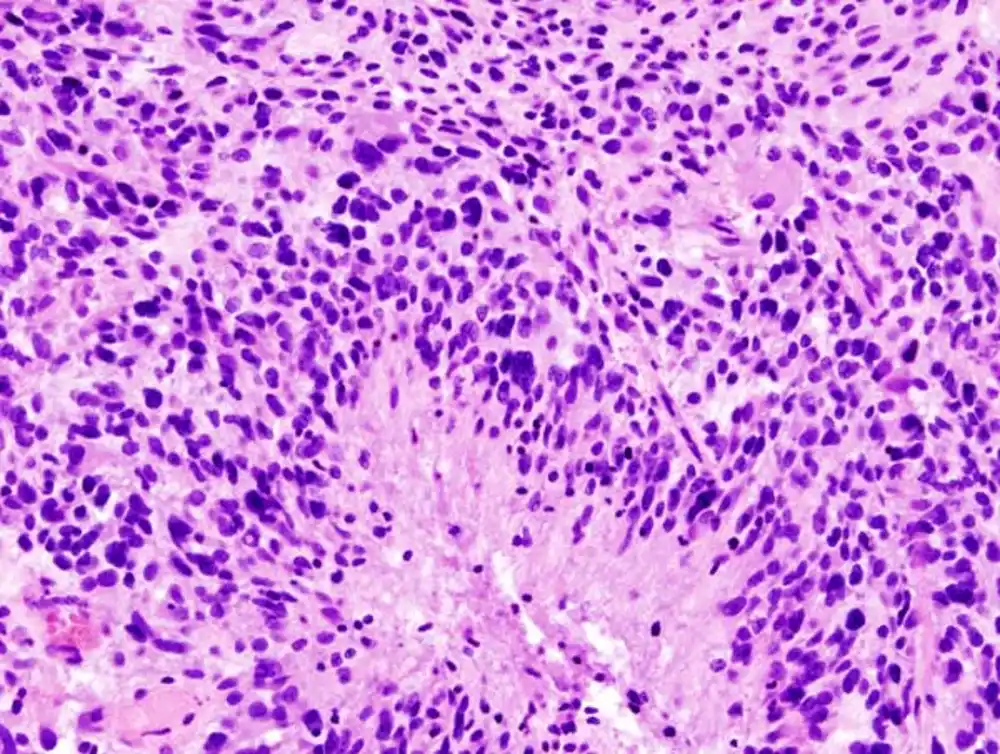
Glioblastom je najčešći i najagresivniji tip primarnog tumora mozga, sa prosečnom stopom preživljavanja od 15 meseci, prema Centrima za kontrolu i prevenciju bolesti. Dok se glioblastom može dijagnostikovati u bilo kom uzrastu, on se prvenstveno dijagnostikuje kod starijih osoba koje imaju prosečnu starost od 65 godina, prema Nacionalnom društvu za tumore mozga.
Glioblastom se formira iz astrocita, koji čine većinu ćelija u centralnom nervnom sistemu. Rak je poznat po tome što brzo metastazira u druge delove mozga, što može da naruši fizičko, emocionalno i kognitivno funkcionisanje osobe i ograniči njihovu sposobnost da obavlja svakodnevne zadatke.
Prosečna dužina preživljavanja za glioblastom nije uspela da se poboljša otkako je prvi put identifikovan u naučnoj literaturi pre skoro 100 godina. Uprkos tome, naučnici u Sveobuhvatnom centru za rak Robert H. Lurie Univerziteta Northvestern ostaju nepokolebljivi u svojoj posvećenosti poboljšanju razumevanja i lečenja glioblastoma kroz rigorozne istraživačke inicijative i klinička ispitivanja.
Istorijski gledano, loš odgovor glioblastoma na lečenje se pripisuje heterogenosti i evoluciji tumora, što pomaže tumoru da se odupre lečenju, što uključuje operaciju praćenu kombinacijom agresivne hemoterapije i zračenja.
Kao odgovor, više istraživača Feinberga pokušalo je da identifikuje nove mehanizme koji doprinose rastu tumora glioblastoma, što može pomoći u prilagođavanju razvoja novih strategija precizne medicine.
„Ovu bolest promoviše hipoksična niša koja pokreće nekoliko aspekata rasta tumora i otpornosti na terapiju, a razumevanje mehanizama koji stoje iza njenog rasta može dovesti do novih terapija“, rekao je dr Džejson Miska, docent neurološke hirurgije.
Jedan od ovih mehanizama koje je Miska nedavno otkrio i objavljen u časopisu Cell Metabolism uključuje novi mehanizam „hranjenja“ koji koriste specijalizovane imune ćelije unutar mikrookruženja tumora glioblastoma, nazvane mijeloidne ćelije povezane sa tumorom, za promovisanje rasta tumora i otpornosti na lečenje.
Miskini nalazi sugerišu da ciljanje ovih ćelija i inhibiranje ovog mehanizma „hranjenja“ može biti obećavajuća strategija lečenja za usporavanje progresije tumora i poboljšanje odgovora na lečenje, kaže Miska.
„Kreatin koji se hrani glioblastomom povećava njihov opstanak pod stresom, promoviše fenotipove matičnih ćelija i na kraju doprinosi progresiji tumora“, rekla je Miska.
Da bi efikasnije identifikovali ove nove mehanizme, istraživači predvođeni dr Feng Jueom, profesorom molekularne medicine Duane i Suzan Burnham, razvili su prvi interaktivni 3D prostorni pristup te vrste kako bi obezbedili sveobuhvatan tri- dimenzionalni prikaz tumora glioblastoma.
Pristup, detaljno opisan u nedavnoj studiji objavljenoj u časopisu Cell, omogućava naučnicima da proučavaju genetske mutacije u celom tumoru, koji se istorijski oslanjao na biopsije jednog tkiva koje mogu da karakterišu samo jednu oblast tumora u isto vreme.
„Ideja je da ako pronađemo jednu mutaciju koja se pojavljuje na svim različitim mestima istog tumora, veća je verovatnoća da će ta mutacija biti pokretačka mutacija ili događaj inicijacije raka. Ali ako proučavamo samo jedno mesto tumora, verovatno smo pobedili „Nemam tako jasan pogled na klonsku inicijaciju i proces evolucije“, rekao je Iue, profesor biohemije i molekularne genetike, patologije i direktor Centra za naprednu molekularnu analizu. „Kroz ove vrste studija, u mogućnosti smo da identifikujemo mnoge nove fuzije koje su propustile druge platforme. Neke od njih čak mogu biti meta lekova koje je odobrila FDA.“
Pored direktnog lečenja tumora operacijom, hemoterapijom i zračenjem, mobilizacija imunog sistema tela je ključna u kontekstu glioblastoma, jer ograničene T-ćelije postoje u mikrookruženju tumora, rekla je Ejmi Hajmberger, MD, Ph.D., Jean Malnati Miller Profesor za istraživanje tumora mozga, potpredsednik za istraživanje na Odeljenju za neurološke hirurgije.
U nedavnoj studiji koju su zajedno vodili Heimberger i saradnici sa Univerziteta Teksas MD Anderson Cancer Center, naučnici su otkrili da korišćenje novog agonista leka za ciljanje STING (stimulator gena interferona) puta u ćelijama glioblastoma može reprogramirati prethodno potisnute imune odgovore.
„Pokazali smo da terapijska aktivacija STING puta u mikrookruženju glioma značajno reprogramira imunološku populaciju“, rekla je Hinda Najem, MD, MS, postdoktorski saradnik u laboratoriji Heimberger i koautor studije. „Ovi istaknuti nalazi zaslužuju razmatranje za ljudski klinički prevod.“
Drugi pristup u poboljšanju odgovora na lečenje glioblastoma može biti iskorištavanje B-ćelija za borbu protiv tumora, prema nedavnoj studiji objavljenoj u Journal of Clinical Investigation i koju vodi Catalina Lee-Chang, Ph.D., docentka neurološke hirurgije.
U studiji, Li-Čangov tim je procenio efikasnost B-ćelijskih vakcina i antitela koja ona promovišu u borbi protiv tumora glioblastoma. Na mišjim modelima glioblastoma, naučnici su otkrili da su vakcine bile u stanju da efikasno infiltriraju tumor i proizvode jedinstvena antitela koja inhibiraju migraciju ćelija glioblastoma i invaziju zdravih moždanih ćelija kod miševa.
„Najznačajniji nalaz ovde je potvrda da naše terapije B-ćelijama ne samo da mogu da aktiviraju CD8 T-ćelije koje ubijaju tumor, već i njihov podskup može da se infiltrira u tumor i proizvede terapeutska antitela. Sada imamo naučni dokaz da ovaj novi B -ćelijske terapije proizvode terapeutska antitela koja mogu inhibirati rast glioblastoma“, rekao je Lee-Chang.
Drugi pristup koji su razvili Lee-Chang i Adam Sonabend, MD, vanredni profesor neurološke hirurgije, koristio je ultrazvučnu tehnologiju da prodre kroz krvno-moždanu barijeru i obezbedi malu dozu hemoterapije i antitela na kontrolnoj tački imunog sistema kako bi se ponovo aktiviralo prepoznavanje glioblastoma od strane imunog sistema. tumorske ćelije.
„Ovo bi mogao biti veliki napredak u lečenju glioblastoma, koji je bio frustrirajuće težak rak za lečenje, delom zbog lošeg prodora cirkulišućih lekova i antitela u mozak“, rekao je Sonabend.
Prvi pristup ove vrste, detaljno opisan u studiji objavljenoj u Nature Communications, koristi ultrazvučni uređaj za implantaciju lobanje koji može poboljšati prodiranje leka za hemoterapiju doksorubicin i antitela za blokadu imunološke kontrolne tačke u mozak tako što proizvodi mikromehuriće koji se privremeno otvaraju. krvno-moždanu barijeru, omogućavajući imunoterapiji da uđe u mozak.
„Ovo je sjajan primer translacionog istraživanja od klupe do kreveta, leđa do klupe, koje postavlja izuzetan scenario za učenje o sposobnosti imunog sistema da ubija tumore mozga u realnom vremenu nakon lečenja“, rekao je Li- Chang. „S obzirom na nedostatak efikasnog imunološkog odgovora protiv ovih smrtonosnih tumora, ovi nalazi nas podstiču da zamislimo potencijalni novi pristup lečenju.“