U stalnim naporima da poboljšaju opioidne lekove protiv bolova, američki i kineski naučnici su koristili crioEM tehnologiju da reše detaljne strukture cele porodice opioidnih receptora vezanih za njihove peptide koji se pojavljuju u prirodi. Potom su sprovedene naknadne biohemijske studije vođene strukturom da bi se bolje razumeli mehanizmi selektivnosti peptidnih receptora i signalnih lekova.
Ovaj rad, objavljen u Cell, pruža sveobuhvatan strukturni okvir koji bi trebalo da pomogne proizvođačima lekova da racionalno dizajniraju bezbednije lekove za ublažavanje jakog bola.
Ovaj rad je predvodila laboratorija dr Erica Ksua, u CAS Kei Lab za istraživanje receptora u Kini, u saradnji sa laboratorijom dr Brajana L. Rota, doktora nauka, na UNC School of Medicina, gde je diplomirani student Džef DiBerto vodio farmakološke eksperimente da bi razumeo mehanizme signalizacije receptora.
Opioidni lekovi ublažavaju bol oponašajući prirodnu funkciju ublažavanja bola unutar naših nervnih simptoma. Oni su najbolji, najjači lekovi protiv bolova koje imamo. Nažalost, oni dolaze sa neželjenim efektima, od kojih su neki ozbiljni kao što su ukočenost, zavisnost i respiratorna depresija, što dovodi do smrti od predoziranja.
Naučnici već dugi niz godina pokušavaju da prevaziđu problem nuspojava na različite načine, a svi uključuju jedan ili više od četiri opioidna receptora, ali bezuspešno. Jedan od načina na koji naučnici nastavljaju da istražuju je stvaranje peptida ili lekova sa malim molekulima inspirisanih peptidima.
Peptidi su kratki lanci aminokiselina; zamislite ih kao kratke proteine. Određeni prirodni ili endogeni peptidi se vezuju za opioidne receptore na površini ćelija da bi stvorili analgetički efekat, takođe poznat kao ublažavanje bolova. Zamislite analgetik kao anestetik, osim što analgetici ne „isključuju“ nerve da bi utrnuli telo ili promenili svest. Dakle, ideja je da se stvori peptidni lek koji ima snažan analgetički efekat, bez umrtvljivanja nerava ili promene svesti ili izazivanja problema sa varenjem, disajnim putevima ili bolestima zavisnosti.
„Problem u ovoj oblasti je što nam je nedostajalo molekularno razumevanje interakcije između opioidnih peptida i njihovih receptora“, rekao je Rot, ko-stariji autor i uvaženi profesor farmakologije Majkla Hukera. „Trebalo nam je ovo razumevanje kako bismo pokušali da racionalno dizajniramo moćne i bezbedne peptide ili lekove inspirisane peptidima.“
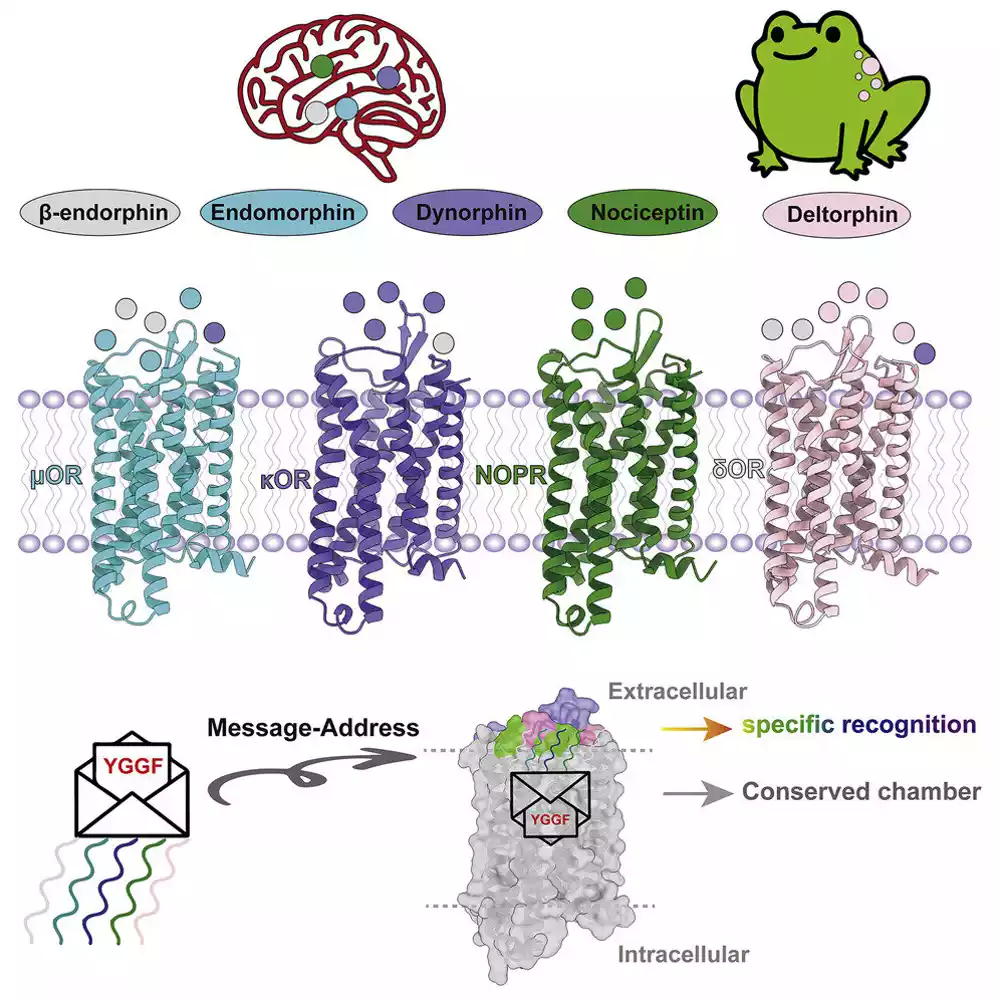
Koristeći kriogenu elektronsku mikroskopiju, ili crioEM, i bateriju biomehaničkih eksperimenata u ćelijama, laboratorije Ksu i Roth sistematski su rešavale detaljne strukture endogenih peptida vezanih za sva četiri opioidna receptora. Ove strukture su otkrile detalje i uvid u to kako specifični opioidni peptidi koji se javljaju u prirodi selektivno prepoznaju i aktiviraju opioidne receptore. Istraživači su takođe koristili egzogene peptide, ili jedinjenja slična lekovima, u nekim od svojih eksperimenata da bi saznali kako oni aktiviraju receptore.
KrioEM strukture receptora vezanih za agoniste u kompleksu sa njihovim efektorima G proteina (nazvanim njihovo „aktivno stanje“) predstavljaju kako ovi receptori izgledaju kada signaliziraju u ćelijama, dajući detaljan prikaz interakcija peptid-receptor. Roth laboratorija je koristila strukture koje je rešila Ksu laboratorija da bi vodila dizajn mutantnih receptora, a zatim je testirala ove receptore u biohemijskim testovima u ćelijama da bi utvrdila kako oni menjaju signalizaciju receptora. Razumevanje ovih interakcija se zatim može koristiti za dizajniranje lekova koji su selektivni za podtipove opioidnih receptora, kao i za proizvodnju određenih signalnih ishoda koji mogu biti korisniji od onih kod konvencionalnih opioida.
„Ova saradnja je otkrila očuvane, ili zajedničke, mehanizme aktivacije i prepoznavanja sva četiri opioidna receptora, kao i razlike u prepoznavanju peptida koji se mogu iskoristiti za kreiranje podtipova selektivnih lekova“, rekao je DiBerto, prvi autor i dr. kandidat u Roth laboratoriji. „Pružamo više potrebnih informacija da nastavimo da guramo polje napred, da odgovorimo na osnovna naučna pitanja na koja do sada nismo mogli da odgovorimo.
Prethodna istraživanja su pokazala strukturu opioidnih receptora u njihovim neaktivnim ili aktivnim stanjima, pri čemu strukture aktivnog stanja postoje samo za podtip mu-opioidnih receptora, primarni cilj lekova kao što su fentanil i morfijum. U radu Cell, autori pokazuju receptore vezane za agoniste u kompleksu sa njihovim efektorima G proteina, što je omogućeno pomoću crioEM tehnologije koja nije postojala kada su se razvijali lekovi koji se trenutno koriste.
Lekovi kao što su oksikontin, oksikodon i morfijum izazivaju različite efekte unutar ćelija i kroz nervni simptom, uključujući ublažavanje bolova. Ali oni takođe imaju efekte na probavni i respiratorni sistem i u interakciji sa ćelijama dovode do zavisnosti. Fentanil je, u međuvremenu, još jedan moćan lek za ublažavanje bolova, ali se vezuje za opioidne receptore na takav način da izaziva ozbiljne neželjene efekte, uključujući gašenje respiratornog sistema.
Potisak iza takvog istraživanja koje su vodili Ksu i Rot je da se ukažu na mehaničke razloge za potenciju ublažavanja bolova bez pokretanja ćelijskih mehanizama koji dovode do ozbiljnih neželjenih efekata i predoziranja.
„Pokušavamo da napravimo bolju vrstu opioida“, kaže Rot, „nikada nećemo stići tamo bez ove vrste osnovnih molekularnih uvida, u kojima možemo da vidimo zašto se bol ublažava i zašto se javljaju neželjeni efekti.