Biolozi matičnih ćelija sa Harvarda uveli su revolucionarnu metodu 3D organoidne kulture za generisanje velikog broja satelitskih ćelija odraslih skeletnih mišića, takođe poznatih kao mišićne matične ćelije, in vitro.
Očekuje se da će sposobnost efikasnog stvaranja funkcionalnih mišićnih matičnih ćelija na ovaj način ubrzati razumevanje i lečenje poremećaja skeletnih mišića, uključujući i one neuromišićnog porekla. Nova tehnika, detaljno opisana u Nature Biotechnology, takođe pruža moćno sredstvo za proučavanje biologije mišića.
„Ljudi će moći da izvode sve ove eksperimente sa presađivanjem i regeneracijom jer odjednom imate milione ćelija“, rekao je koautor i naučnik sa Harvarda Feodor Prajs. „Idite da se igrate sa njima, proučavajte ih, pogledajte svoje omiljene gene i puteve u svojim laboratorijama.“
Prajs je radio sa Li Rubinom, profesorom na Odeljenju za matične ćelije i regenerativnu biologiju i kopredsedavajućim Programa za bolesti nervnog sistema Harvardskog instituta za matične ćelije, kako bi bio pionir u laboratorijskim satelitskim ćelijama koje su veoma slične izvornim odraslim matičnim ćelijama i odgovorne su za rast i regeneraciju skeletnih mišića.
Njihov jedinstveni pristup prevazilazi izazov održavanja regenerativnih sposobnosti satelitskih ćelija kada se kultivišu van tela tradicionalnim metodama. „Kada ih izvadite iz tela, one u suštini prestaju da budu matične ćelije“, objasnio je Prajs.
Prajs objašnjava da kada se kultivišu satelitske ćelije sa ciljem povećanja njihovog broja, one se brzo razmnožavaju, ali se onda spontano diferenciraju u mioblaste (mišićne progenitorne ćelije), gubeći svoj prvobitni funkcionalni kapacitet satelitskih ćelija. Ovo dovodi do neefikasne popravke i održavanja mišića kada se ćelije ponovo transplantiraju u telo.
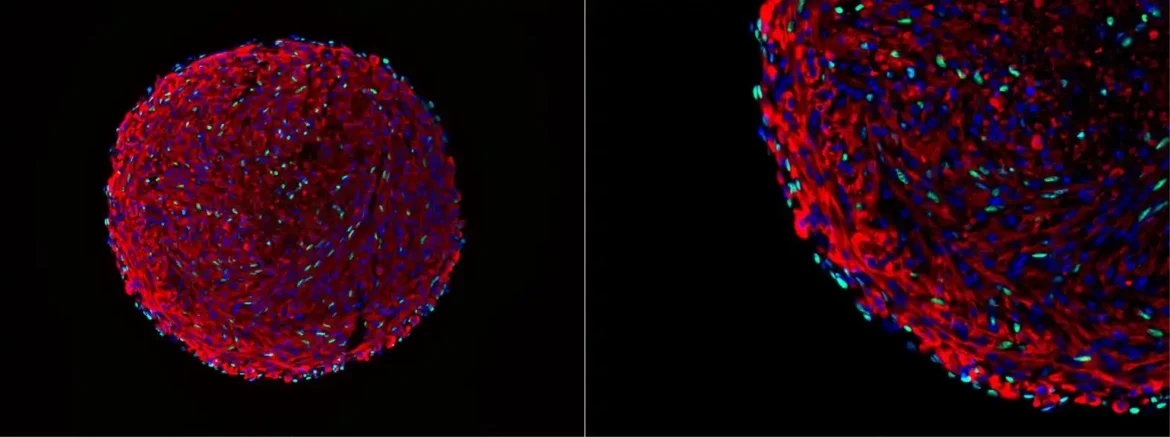
Proboj Harvardskog tima u održavanju regenerativnih sposobnosti satelitskih ćelija proizašao je iz inovativne upotrebe tehnika 3D kulture organoida. Stavljanjem mioblasta miša u bočice za centrifugiranje, istraživači su mogli da generišu organoide koji sadrže diferencirana mišićna vlakna i populaciju ćelija koje eksprimiraju ključni satelitski ćelijski marker Pak7.
Prisustvo ovog važnog faktora transkripcije i organizacija strukture unutar organoida bili su pokazatelji uspeha njihove metode.
„Uvereni smo da smo uspešno rekonstruisali nišu satelitske ćelije“, rekao je Prajs, „i zbog toga smo uspeli da nateramo ćelije unutar tog organoida da se vrate u stanje satelitske ćelije. U suštini, stvorili smo satelitske ćelije in vitro, značajno dostignuće koje obećava veliko polje regenerativne medicine i biologije mišića.“
Opsežna in vitro i in vivo karakterizacija pokazala je da ove matične ćelije veoma liče na verodostojne satelitske ćelije, uključujući njihovu malu veličinu, mirovanje i obrasce ekspresije ključnih gena i epigenetskih oznaka. One, međutim, nisu identične nativnim ćelijama. Analiza RNK i DNK otkrila je da ćelije generisane u laboratoriji imaju srednji transkripcioni i epigenetski profil između satelitskih ćelija i mioblasta.
Ono što je najvažnije, kada su transplantirane u mišić miša, ćelije su bile u stanju da se usade, ponovo nasele nišu matičnih ćelija, opstanu dugoročno i regenerišu mišiće nakon ponovljenih povreda – sve ključne funkcije nativnih satelitskih ćelija.
U jednom eksperimentu, istraživači su pokazali da je transplantacija novih ćelija, ali ne i mioblasta, u ozračeni mišić miša bez endogenih satelitskih ćelija dovela do regeneracije mišića sa normalnom kontraktilnom silom. Mioblasti su uradili tačno ono što se očekivalo: ništa. Nisu napravili mišiće.
U poređenju sa tim, matične ćelije i satelitske ćelije su napravile pristojne mišiće. „Kada smo uporedili njihovu sposobnost kontrakcije, bili smo oduševljeni što smo u suštini videli da je generisanje sile iz tog kontraktilnog mišića identično“, rekao je Prajs.
Dodao je: „Nije me toliko impresionira sposobnost ćelija da se usade. To je njihova sposobnost da ponovo nasele nišu matičnih ćelija, jer ako to urade, one će se usaditi i opstati dugoročno.“
Istraživači su takođe bili u mogućnosti da generišu satelitske ćelije iz ljudskih mioblasta, uključujući visoko-pasirane komercijalne ćelijske linije. Ovo ima važne implikacije za razvoj ćelijskih terapija, pošto je rad sa ljudskim tkivom težak, a veliki broj funkcionalnih ćelija sličnih satelitima sada se može proizvesti in vitro.
Ovo istraživanje je podržao Blavatnik Biomedical Accelerator i strateški savez između Univerziteta Harvard i National Resilience koji je osnovala Harvardova kancelarija za tehnološki razvoj (OTD) kako bi unapredila istraživanje ka mogućnostima komercijalizacije.
Nadovezujući se na ovaj napredak, istraživački tim je postavio osnovu za projekat saradnje sa drugim laboratorijama na Harvardu za modelovanje celog neuromišićnog kola, sa potencijalnim primenama za stanja kao što su spinalna mišićna atrofija, ALS i facioskapulohumeralna mišićna distrofija.
„Naša laboratorija je provela godine radeći na ‘neuralnoj’ strani neuromišićnih bolesti“, rekao je Rubin. „Sada se radujemo vremenu kada ćemo moći da generišemo potpuno novo kolo koje se proteže od kičmene moždine do visoko funkcionalnih mišića.“