Precizna segregacija DNK i verno nasleđe plazmida su ključni koraci u deobi bakterijskih ćelija. Sada je tim istraživača predvođen Šonom Marejem sa Instituta Maks Plank za zemaljsku mikrobiologiju razvio računarsku simulaciju koja objašnjava ključni mehanizam segregacije DNK. Njihovi nalazi otvaraju put za eksperimentalno testiranje i otkrivaju fundamentalne biohemijske principe relevantne za sintetičku biologiju i medicinsku primenu.
Verno nasleđe genetskog materijala sledećoj generaciji je fundamentalni proces koji leži u osnovi svih oblika života. Centralno za ovaj proces je precizan prenos kopiranog genetskog materijala tokom ćelijske deobe.
Istraživački tim koji predvodi Sean Murrai sa Instituta Maks Plank za zemaljsku mikrobiologiju je sada uspešno razvio računarsku simulaciju za ovaj centralni proces. Za razliku od eksperimentalnih tehnika, koje su često ograničene svojom rezolucijom, stohastičko modeliranje omogućava da se otkriju osnovni procesi segregacije DNK i da se razume fina struktura uključenih proteina.
Suštinski deo ovog procesa, kod mnogih bakterija, je formiranje velikog makromolekularnog kompleksa koji se naziva particioni kompleks, koji se formira kao deo ParABS sistema. Ovde ParB protein deluje tako što pomera DNK kroz interakciju sa ParA-ATP-vezanim za DNK, omogućavajući tako aktivno odvajanje DNK. Za pravilno funkcionisanje zahteva precizne interakcije između njegovih proteinskih poddelova i DNK.
Uprkos njihovom značaju, i struktura proteinskih kompleksa i mehanizmi koji stoje iza njihovog sklapanja ostali su neuhvatljivi. Nadovezujući se na nedavna otkrića, istraživački tim je razvio model koji pokazuje da DNK i ParB dimeri mogu pratiti princip „klizanja i premošćavanja“.
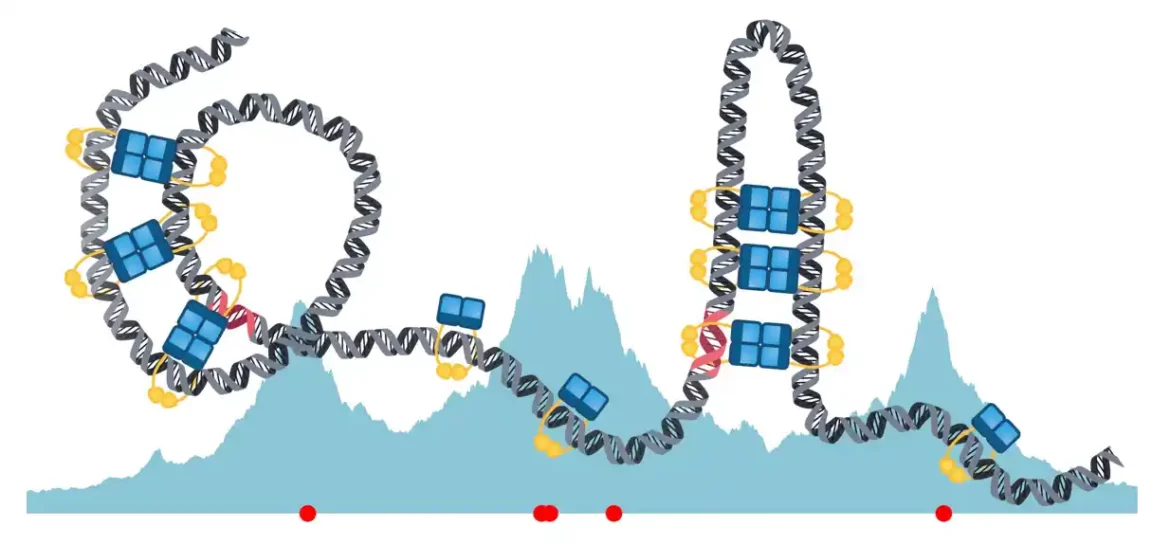
Diplomirani student Lara Connollei, prvi autor studije, fokusirala se na proces učitavanja ParB dimera na DNK, koji se javlja u specifičnim regionima poznatim kao parS mesta. „Prema našem stohastičkom modelu, ParB dimeri se vežu za DNK na parS mestima formiranjem proteinske stezaljke, a zatim klize duž lanca DNK, slično kao perle na lancu. Takođe predviđamo da kratkotrajni mostovi organizuju DNK u ukosnicu i spiralne strukture za kondenzaciju DNK. Štaviše, ovi mostovi ne ometaju klizanje“, objašnjava Lara Konoli.
Vođa istraživačke grupe Šon Marej dodaje: „Interakcije premošćavanja između dimera dovode do savijanja DNK i formiranja različitih struktura. Dalja istraživanja ovih strukturnih varijacija mogu potencijalno biti ključ za razumevanje uloge ParB u različitim biološkim kontekstima.“ Studija otvara vrata za dalja istraživanja i eksperimentisanje kako bi se nadovezali na nalaze.
Sledeći korak je izvođenje eksperimenata za detaljnije testiranje i validaciju predviđanja modela. Pored toga, studije različitih vrsta bakterija bi pomogle da se bolje razume raznolikost prisutna u strukturi kompleksa pregrada.
„Naša studija pruža dublji uvid u svet segregacije DNK i potencijalno je relevantna za mnoge različite bakterijske vrste, kao i za plazmide sa malim brojem kopija, koje takođe izdvaja ParABS sistem“, kaže naučnik Maks Plank Šon Marej. „Geni otpornosti na antibiotike nalaze se na takvim plazmidima. Stoga, osim što su važni kao osnovno istraživanje, ovi rezultati bi mogli biti važni i za javno zdravlje.“
Nalazi su objavljeni u časopisu Nature Communications.