U 2015. godini, izbijanje Zika virusa, izazvano jakom kišnom sezonom i kasnijim procvatom populacije komaraca domaćina virusa, dovela je do toga da se hiljade beba u Brazilu rodi sa teškim urođenim manama. Zika virus je jedinstven među flavivirusima, koji takođe uključuju viruse Zapadnog Nila, denga i žute groznice, po svojoj sposobnosti da se prenesu sa zaražene majke na njeno nerođeno dete.
Kako se komponente Zika virusa okupljaju tokom replikacije virusa i kako virus onda prelazi sa majke na fetus? Ovo su neka od pitanja na koja Joice Jose, docent za biohemiju i molekularnu biologiju u Penn State-u, i njene kolege žele da odgovore.
„Dok je broj infekcija zika virusom kod ljudi opao od razorne epidemije 2015. godine, opasnost od budućih epidemija i dalje ostaje“, rekao je Hoze. „A sa klimatskim promenama, komarci koji nose Zika virus mogu da pomere svoje domete ka severu, što bi moglo da dovede još više ljudi, uključujući i SAD, u veći rizik. S obzirom da trenutno ne postoje vakcine ili antivirusne terapije, važno je proučavanje virusa u cilju informisanja razvoja mera prevencije“.
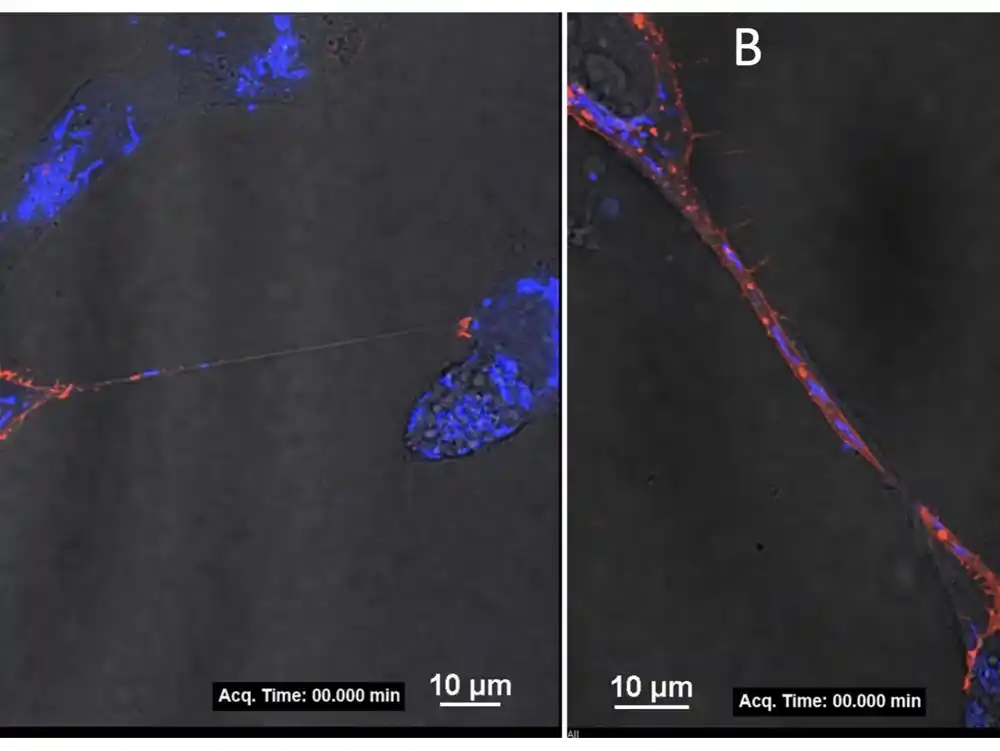
Hoze je objasnila da su ona i njene kolege nedavno otkrile da ćelije majke zaražene Zika virusom stvaraju veze, nazvane tunelske nanocevi, koje se protežu do neinficiranih ćelija, kako unutar majke, tako i od majke do fetusa. Nalazi te studije su trenutno u fazi revizije i javno su dostupni u formi za štampu.
„Mislimo da ove tunelske nanocevi omogućavaju virusu da se replicira u majci i da pređe sa majke na bebu“, rekao je Hoze. „Pored obezbeđivanja mehanizma za prolazak kroz placentu, ove nanocevi mogu omogućiti virusu da izbegne imuni odgovor domaćina. Ovo nazivamo prikrivenim načinom prenosa.“
U svom prethodnom istraživanju, tim je otkrio da određeni protein, nazvan nestrukturni protein 1 (NS1), može biti odgovoran za izazivanje formiranja ovih nanocevi. Jose i njena koleginica Indira Misorekar, profesorica medicine na Bailor College of Medicine, sprovešće eksperimente na ljudskim ćelijama in vitro, što znači u posudi za kulturu, i in vivo, što znači na živim miševima, kako bi ispitali specifične regione NS1 koji mogu učestvovati u signaliziranju ili interakciji sa proteinima na ljudskim ćelijama kako bi se pokrenulo formiranje nanocevi.
„Otkrivanje toga koji regioni NS1 „razgovaraju“ sa ljudskim proteinima je prvi korak u razumevanju kako počinje formiranje nanocevi“, rekao je Hoze. „Ako možemo da shvatimo kako ovaj protein funkcioniše, možemo potencijalno ciljati protein lekovima koji onemogućavaju njegovu funkciju. Zanimljivo je da kada sam bio postdoktor, moja laboratorija je bila ključna u rešavanju strukture virusa denga NS1, tako da sada Vratio sam se svojim korenima da dalje proučavam ovaj važan protein.“
Zatim će istraživači proučiti da li se cele čestice virusa ili samo virusna RNK, ili genetski materijal, transportuju kroz nanocevi.
„U našem prethodnom istraživanju, dokumentovali smo komponente virusa, poput RNK i određenih proteina, unutar ovih nanocevi, tako da je pitanje da li ceo virus ili samo komponente virusa mogu da prođu kroz njih“, rekao je Hoze.
Pored toga, istraživači planiraju da dalje istraže ulogu formiranja tunelskih nanocevi u prenošenju Zika virusa sa majke na fetus ispitivanjem virusa u akciji kod trudnih miševa. Konačno, tim će proučavati transport mitohondrija kroz ove nanocevi.