U početku se svaka matična ćelija suočava sa sudbonosnim izborom. Tokom razvoja kože, na primer, embrionalni epidermis počinje kao jedan sloj epidermalnih progenitornih ćelija. Njihov izbor je da postanu zrela epidermalna ćelija ili da pređu na ćeliju folikula dlake. Ovim takozvanim prebacivanjem sudbine upravlja faktor transkripcije SOX9. Ako progenitorska ćelija eksprimira SOX9, razvijaju se ćelije folikula dlake. Ako nije, rade epidermalne ćelije.
Ali postoji tamna strana SOX9, jer je umešan u mnoge od najsmrtonosnijih karcinoma širom sveta, uključujući rak pluća, kože, glave i vrata i kostiju. U koži, neke aberantne odrasle epidermalne matične ćelije kasnije uključuju SOX9 uprkos svom izabranom putu – i nikada ga ne isključuju, pokrećući proces koji na kraju aktivira gene raka.
Naučnici nikada nisu u potpunosti razumeli kako ovaj osuđeni ishod dolazi na molekularnom nivou. Ali sada su Rokfelerovi istraživači otkrili mehanizme iza ovog zloćudnog preokreta. SOX9, kako se ispostavilo, pripada posebnoj klasi proteina koji upravljaju prenosom genetskih informacija sa DNK na iRNK. To znači da ima sposobnost da otvori zapečaćene džepove genetskog materijala, da se veže za prethodno tihe gene unutar i da ih aktivira. Objavili su svoje rezultate u Nature Cell Biologi.
„Naše otkriće pruža nove uvide u to kako rak izbacuje pažljivo podešen proces donošenja odluka matične ćelije, nakon čega onemogućava stvaranje normalnog tkiva“, kaže Elejn Fuks, šef laboratorije Robin Čemers Nojštajn za biologiju i razvoj ćelija sisara. „Takođe osvetljava nove gene aktivirane SOX9 kao potencijalne terapeutske mete.“
Naš genom nije otvorena knjiga. U stvari, to više liči na biblioteku ispunjenu nekoliko milijardi knjiga koje su uglavnom pod ključem – većina genetskog materijala zapravo leži u tišini unutar nekodirajućih i čvrsto povezanih paketa DNK ograđenih histonskim proteinima u zatvorenom prostoru. država. Zajedno DNK i histoni formiraju ono što se zove zatvoreni hromatin. Geni koji su upakovani u ovaj zatvoreni materijal su nedostupni transkripcionim proteinima, ili faktorima, koji bi mu pomogli da eksprimira gene unutar.
Ali postoji nekoliko retkih ključeva koji nisu samo faktori transkripcije. Ovi „pionirski faktori“ mogu otključati te genetske pakete. Oni poseduju supermoć da zavire unutar zatvorenog hromatina i prepoznaju mesta vezivanja unutra. Zatim regrutuju druge faktore transkripcije kako bi im pomogli da otvore zatvoreni hromatin i vežu se za receptorska mesta na nukleozomu, što reprogramira hromatin i aktivira nove gene.
Ovo se obično dešava u ranim fazama razvoja, kada sudbina matične ćelije tek treba da se utvrdi. U odrasloj koži, SOX9 je normalno povezan sa održavanjem identiteta matičnih ćelija folikula dlake odraslih. Obično je potisnut u odraslim epidermalnim matičnim ćelijama. Ali to nije slučaj kada su u pitanju karcinomi bazalnih ćelija i skvamoznih ćelija.
„U kontekstu bolesti, SOX9 se ponovo aktivira u matičnim ćelijama epiderme odraslih“, kaže Jihao Jang, prvi autor studije.
Kako bi se ovaj proces mogao odvijati korak po korak, nije poznato, kaže Jang. „Reprogramiranje in vitro se dešava veoma brzo — u roku od 48 sati. Sa tako kratkim vremenskim okvirom, teško je dobiti dobru rezoluciju o sekvenci događaja.“
Da bi saznali, istraživači su konstruisali miševe koji su sadržali kopiju SOX9 koja bi se mogla aktivirati u njihovim odraslim epidermalnim matičnim ćelijama kada su miševi hranjeni doksiciklinom, lekom koji je indukovao transgeni SOX9.
„U tkivima odraslih, izbori koji su lako napravljeni u embriogenezi su čvrsto potisnuti tako da se odrasle matične ćelije drže svog namenskog zadatka“, objašnjava Fuchs.
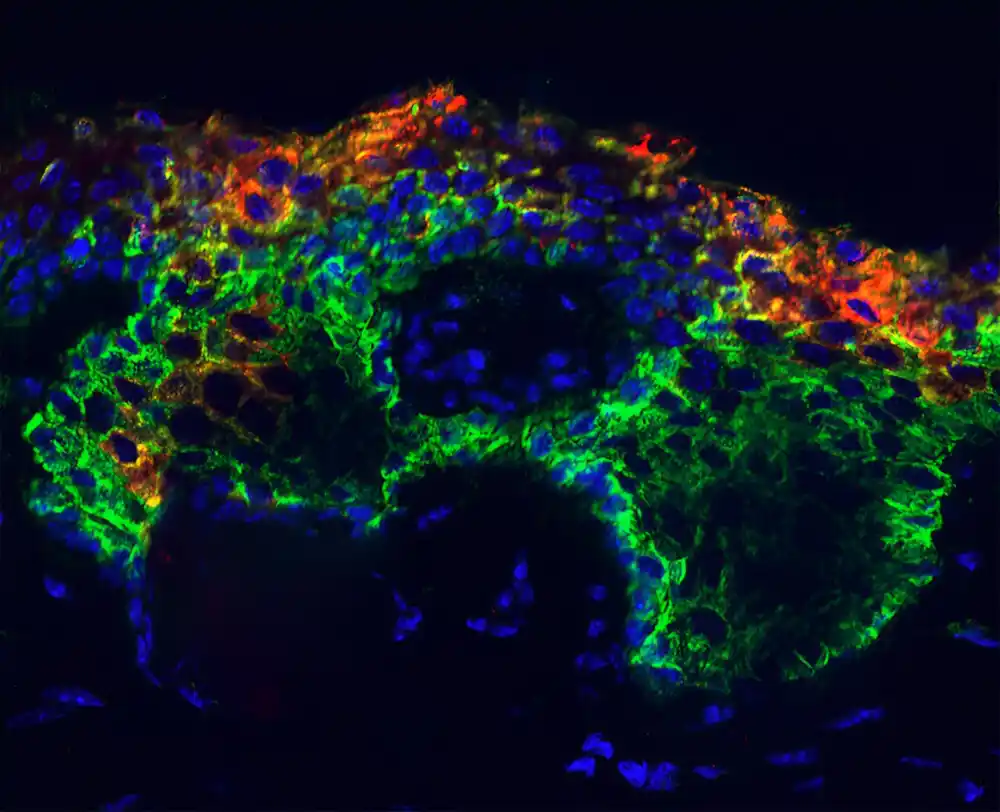
Oslobađanje SOX9, međutim, pokazalo se moćnim uticajem, progresivno reprogramirajući epidermalne matične ćelije za nove sudbine. „Samo izražavanjem ovog pojedinačnog faktora transkripcije SOX9“, kaže Jang, „uspeli smo da indukujemo strukture slične karcinomu bazalnih ćelija do šeste nedelje. Do 12. nedelje smo počeli da viđamo lezije koje su ličile na karcinom bazalnih ćelija kod ljudi.“
Istovremeno su pratili epigenetski proces koji se odvija iza kulisa. U prve dve nedelje, SOX9 je isključio gene epidermalnih matičnih ćelija. Preokrenuvši svoje normalno stanje, počeli su da uključuju gene matičnih ćelija folikula dlake.
Tražeći mehanizam, istraživači su otkrili da je SOX9 oteo nuklearnu mašineriju od aktivnih epidermalnih gena i doveo ovu ukradenu opremu do tihih gena folikula dlake, da bi postigao ovaj prekidač sudbine. Zatim je angažovao druge faktore transkripcije da bi otvorio zatvorenu vezu hromatina sa tihim genima u njima, uključivši ih.
„Kada SOX9 nije mogao da se reguliše, matične ćelije nisu uspele da naprave kosu, već su samo nastavile da se razmnožavaju i aktiviraju nekoliko novih faktora transkripcije, što je na kraju dovelo do stanja karcinoma bazalnih ćelija“, kaže Fuchs.
Ovo komplikovano menjanje identiteta napred-nazad bilo je moguće samo zato što je SOX9 pionirski faktor, kaže Jang. „Samo pionirski faktor ima mogućnost pristupa zatvorenom hromatinu“, ističe on.
Pošto je SOX9 previše aktivan u mnogim od najsmrtonosnijih karcinoma širom sveta, istraživači imaju za cilj da potraže načine da intervenišu u svojoj ulozi u proliferaciji ovih ćelija. „Identifikujući kako se proteini SOX9 u interakciji i njegovi ciljni geni menjaju tokom maligniteta, nadamo se da ćemo uspeti da otkrijemo nove mete lekova za ove vrste raka“, kaže Fuchs.