Povrede mozga uzrokuju široko rasprostranjeno oštećenje moždanog tkiva. Oštećene ćelije počinju da proizvode signalne molekule koji pokreću procese upale, apoptoze — programirane ćelijske smrti — i oksidativnog stresa. Nakon akutne faze (oko jednog dana) dolazi do hronične neuroinflamacije. Može trajati dugo i izazvati sekundarno oštećenje sa negativnim posledicama, uključujući poremećaj u ponašanju i kognitivnu disfunkciju.
Lekari Univerziteta RUDN pokazali su da glijalne ćelije pomažu u ublažavanju neuroinflamacije usled povreda mozga. Tačnije, mali „mehurići“ koje proizvode – vezikule – nose proteine i druga jedinjenja.
„Glijalne ćelije oslobađaju širok spektar fiziološki aktivnih supstanci u ekstracelularnim vezikulama za podršku neuronima. Istražili smo da li je moguće koristiti ekstracelularne vezikule glijalnih ćelija za zaštitu neurona u modelu traumatske povrede mozga“, kaže dr Diana Salikhova, šef Laboratorije za ćelijsku biotehnologiju Univerziteta RUDN.
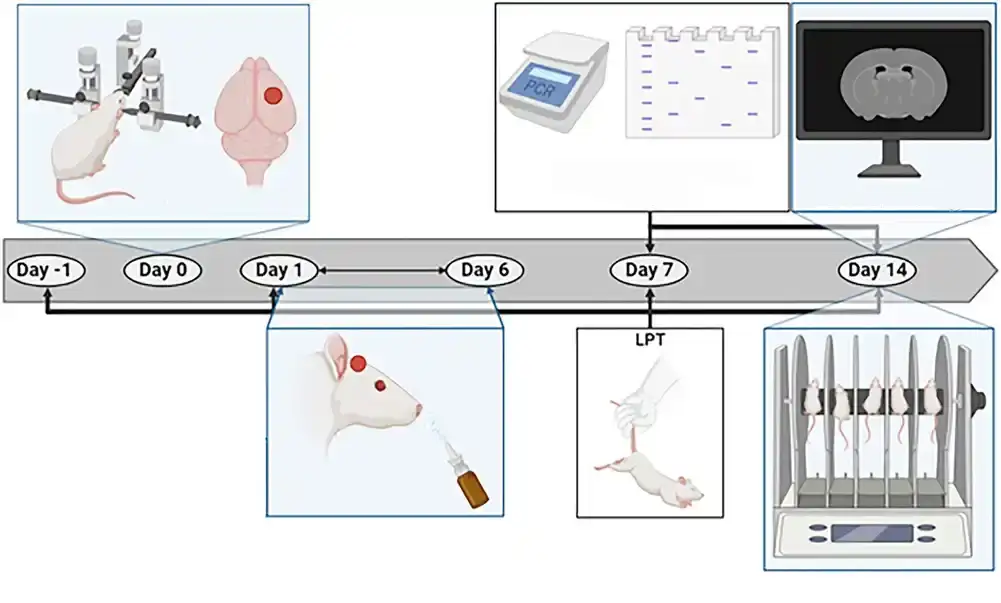
Lekari su eksperimentisali na 30 odraslih pacova. Životinje su hirurški podvrgnute veštačkoj povredi mozga, nakon čega su 15 životinja nakon povrede intranazalno ubrizgane ekstracelularne vezikule glijalnih ćelija. Same glijalne ćelije su dobijene iz indukovanih pluripotentnih matičnih ćelija od zdravih donora. Nedelju dana kasnije, lekari RUDN-a su proverili stanje moždanog tkiva životinja pomoću PCR analize i Vestern blotinga. Posle još nedelju dana, autori su sproveli niz testova kako bi utvrdili karakteristike ponašanja životinja.
Oštećena površina kod životinja koje su primale vezikule se neznatno smanjila – za samo 4 kubna milimetra. Međutim, terapija je doprinela znatno bržem oporavku moždanih funkcija životinja, poboljšanju senzomotornih funkcija oštećene hemisfere i smanjenju upale. Na primer, broj CD68 + makrofaga odgovornih za upalu se tri puta smanjio nakon terapije.
Nivo enzima kaspaze, koji pokreće apoptozu, smanjen je za 2,5 puta. Doktori Univerziteta RUDN otkrili su i molekularni mehanizam koji objašnjava ovaj efekat. Pretpostavlja se da su 203 vrste malih nekodirajućih nukleotidnih sekvenci, mikroRNK, postale agensi neuroprotektivnog delovanja.
„Ekstracelularne vezikule iz glijalnih ćelija pokazale su terapeutske efekte kod traumatskih povreda mozga. Oni su stimulisali oporavak nervnog sistema i neuroplastičnost. Pored toga, pronašli smo 203 tipa mikroRNK, koje se očigledno mogu koristiti za lečenje različitih moždanih patologija“, kaže dr Diana Salikhova. D., šef Laboratorije za ćelijsku biotehnologiju Univerziteta RUDN.