Alchajmerova bolest izaziva značajne probleme sa pamćenjem, razmišljanjem i ponašanjem i najčešći je oblik demencije, koji pogađa više od 50 miliona ljudi širom sveta svake godine. Očekuje se da će se ovaj broj utrostručiti do 2050. godine.
Koristeći sopstvene najsavremenije tehnologije snimanja, naučnici sa Univerziteta Kalifornije u San Dijegu sada su otkrili kako se metabolizam lipida, klase molekula koja uključuje masti, ulja i mnoge hormone, menja kod Alchajmerove bolesti. Takođe su otkrili novu strategiju za ciljanje ovog metaboličkog sistema novim i postojećim lekovima. Nalazi su objavljeni u Cell Metabolism.
„Lipidi su povezani sa Alchajmerovom bolešću otkad znamo za tu bolest“, rekao je stariji i korespondentni autor dr Ksu Čen, docent na Odseku za neuronauke na Medicinskom fakultetu UC San Dijega, pozivajući se na originalni izveštaj Aloisa Alchajmera iz 1907. koji opisuje neobično prisustvo masnih naslaga u mozgu prve osobe kojoj je dijagnostikovana bolest.
„Toliko je naglaska od tada stavljeno na tau i druge proteine da je istraživačka zajednica, do poslednje decenije, u velikoj meri previdela ovaj važan aspekt bolesti.“
„Vođeni velikim interesovanjem za funkcije lipidnih kapljica u starenju i bolestima, pokrenuli smo ovu plodnu saradnju kako bismo iskoristili najsavremeniju SRS tehnologiju za proučavanje metabolizma lipida u mozgovima miša sa tauopatijom“, rekao je Iajuan Li, MD, Ph.D., postdoktor istraživač na Shu Chien-Gene Lai odeljenju za bioinženjering na UC San Diego Jacobs School of Engineering. SRS snimanje je pristup koji analizira način na koji molekuli u uzorku interaguju sa laserskom svetlošću.
U mozgu, lipidi dolaze u obliku sićušnih kapljica koje kontrolišu različite procese, kao što su skladištenje energije i ćelijski odgovori na stres. Ovi procesi su strogo regulisani u tipičnim mozgovima, ali kod Alchajmerove ili sličnih bolesti, metabolizam lipidnih kapljica može da kvari. Dok naučnici shvataju da postoji veza između Alchajmerove bolesti i metabolizma lipida, tačno kako oni utiču jedni na druge ostaje misterija.
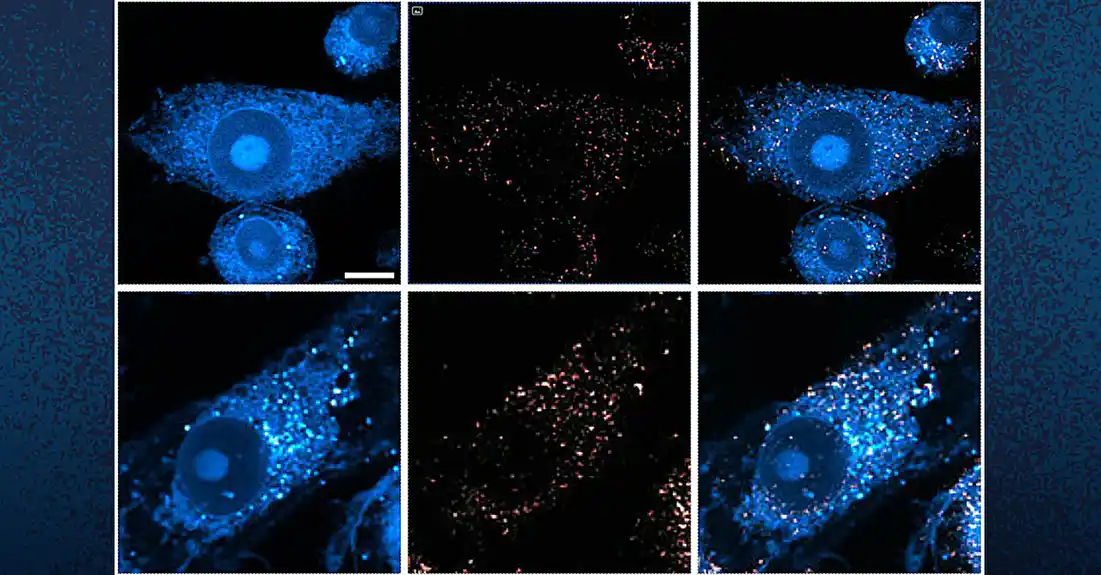
Da bi odgovorio na ovo pitanje, tim je direktno pogledao kapljice lipida u mozgu miševa sa viškom tau proteina. Koristili su najsavremeniju SRS platformu za snimanje koja je razvijena u laboratoriji Lingian Shi na Jacobs School of Engineering. Platforma omogućava snimanje mikroskopskih slika lipidnih kapljica unutar ćelija bez upotrebe hemijskih boja, koje mogu izmeniti delikatne molekule i ugroziti rezultate.
„Intrigantno je to što inertne kapljice lipida primećene u mozgovima tauopatije pokazuju slično ponašanje kao i kod starenja mozga“, rekao je ko-korespondentni autor dr Lingjan Ši, docent za bioinženjering na školi Džejkobs.
„Sada se fokusiramo na razumevanje osnovnih mehanizama tako što ćemo kombinovati SRS snimanje sa drugim korišćenjem multidisciplinarnih tehnika. Naš pristup je biološki neutralan, tako da smo u mogućnosti da posmatramo šta se dešava u mozgu na molekularnom nivou sa što je manje moguće interferencije.“
Ši i njen tim, uključujući Li, su pioniri u novom pristupu, koji koristi posebno modifikovanu verziju vode, nazvanu teška voda, kao metaboličku sondu.
„Umesto da koristimo tipičnu hemijsku boju za bojenje lipida, koristimo tešku vodu koja prirodno učestvuje u metaboličkim aktivnostima za koje smo zainteresovani“, dodao je Ši.
„Ovo nam daje mnogo jasniju sliku o tome kako se lipidi formiraju prostorno-vremenski, što ne bi bilo moguće sa drugim pristupima. Naš trenutni fokus je na razumevanju osnovnih mehanizama ovih dinamičkih promena metabolizma lipida u kontekstu starenja i bolesti.“
Istraživači su otkrili da u mozgu sa tauopatijom, neuroni akumuliraju višak lipida kao rezultat stresa ili oštećenja. Ovaj priliv prisiljava neurone da pretovare višak na imune ćelije u mozgu, koje se nazivaju mikroglija. Ove mikroglije zatim izazivaju inflamatorni odgovor koji uzrokuje dodatni stres neuronima, pokrećući ciklus koji se ponavlja i pogoršava.
Pored karakterizacije ovog procesa, takođe su bili u stanju da identifikuju kritični enzim, nazvan protein kinaza aktivirana adenozin monofosfatom (AMPK) koji orkestrira ciklus. Prema istraživačima, prekid ovog ciklusa mogao bi otvoriti nove mogućnosti lečenja Alchajmerove bolesti. Čen je posebno optimističan u pogledu mogućnosti prenamene postojećih lekova koji modifikuju metabolizam lipida.
„Ne mislimo da je ovo slučajan fenomen“, rekao je Čen. „Dokazi sugerišu da je metabolizam lipida pokretački mehanizam za Alchajmerovu bolest. Postoji mnogo lekova koji ciljaju metabolizam lipida u drugim sistemima tela, kao što je jetra, tako da bismo mogli da promenimo ovaj sistem prilično dramatično koristeći alate koje već imamo.“