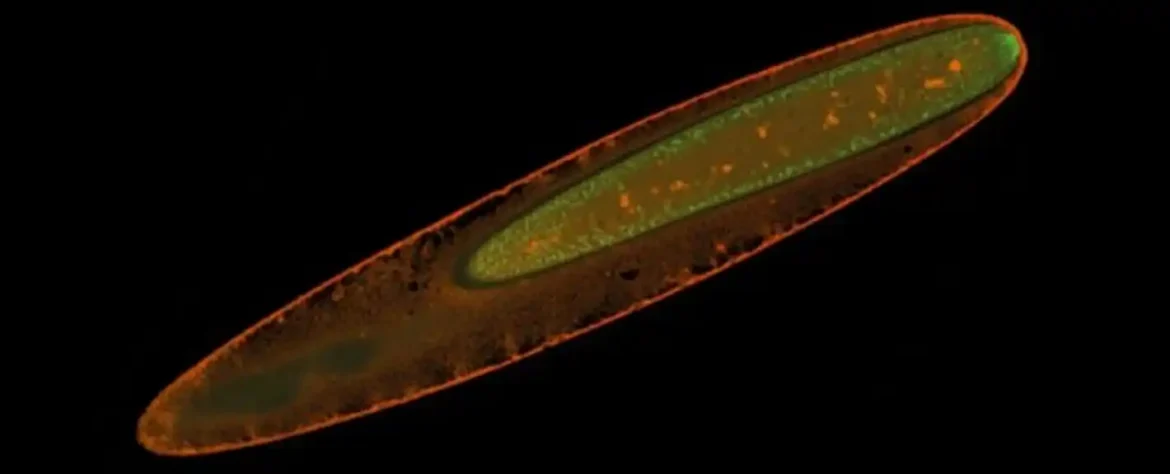
Po prvi put, naučnici su sekvencirali genom misteriozne vrste džinovske bakterije koja se može videti bez mikroskopa.
Otkrića o njihovim reproduktivnim strategijama, mehanizmima preživljavanja i različitim metaboličkim mehanizmima – sličnim mitohondrijama – mogla bi jednog dana biti korisna u razvoju održivih energetskih tehnologija i povećanju efikasnosti u poljoprivredi.
Epulopiscium bakterije žive simbiotski u crevima ribe, Naso tonganus, u okruženju tropskog okeana. Tamo gde je većina bakterija premala da bi se videla bez mikroskopa, ovi jednoćelijski mamuti imaju milion puta veću zapreminu od svojih dobro poznatih rođaka, E. coli, što znači da se mogu uočiti samo golim okom.
„Ova neverovatna džinovska bakterija je jedinstvena i zanimljiva na mnogo načina“, kaže mikrobiolog Ester Angert sa Univerziteta Kornel u SAD. „Otkrivanje genomskog potencijala ovog organizma jednostavno nas je oduševilo.
Prvi član Epulopisciuma – čije ime potiče od latinskih reči za „gost“ i „riba“ – otkriven je 1985.
Angert i njene kolege iz SAD su nazvali vrstu koju su proučavali Epulopiscium viviparus: Druga reč se odnosi na reprodukciju koja dovodi do živorođene dece.
Dok se bakterije obično cepaju na pola da bi napravile dve nove, E. viviparus može napraviti do 12 kopija sebe unutar roditeljske ćelije, koje zatim isplivaju u svet.
Nesposobne da se uzgajaju u laboratoriji, takve džinovske bakterije ostaju kuriozitet biološkog sveta. Da bi proučavali E. viviparus, istraživači su morali da uhvate ribu u kojoj živi i pažljivo sakupe ćelije što je brže moguće za sekvenciranje DNK i analizu transkriptoma.
Većina bakterija ili diše koristeći kiseonik ili dobija energiju iz svog okruženja kroz fermentaciju, što generalno dovodi do manje proizvodnje energije.
E. viviparus je fermentator, ali to je zbunjujuće jer je ogroman, brzo se razmnožava i može da pliva – sve to zahteva relativno velike količine energije.
Izgleda da su bakterije optimizovale svoj metabolizam na okruženje ribljeg creva koje je bogato jonima natrijuma. Protok natrijumovih jona kroz ćelijske membrane stvara moćnu ‘natrijumovu pokretačku silu’ za stvaranje energije i okretanje njihovih dlakastih dodataka zvanih flagele za kretanje.
Ova pokretačka sila natrijuma takođe pokreće kretanje flagela kod Vibrio cholerae, bakterija koje izazivaju koleru.
Tim je takođe otkrio da veliki deo genetskog koda E. viviparus stvara enzime koji su veoma efikasni u ekstrakciji hranljivih materija iz riba domaćina, posebno ugljenih hidrata koji se nazivaju polisaharidi iz algi koje čine veliki deo ishrane N. tonganus.
E. viviparus ima obilje enzima koji takođe stvaraju ATP, ‘energetsku valutu’ koja podržava širok spektar ćelijskih procesa. Otkrili su prostor za ove molekule u jedinstvenoj membrani, sličnoj mitohondrijama složenijih organizama.
„Svi znamo onu frazu „mitohondrije su moć ćelije“, i začuđujuće je da su se ove membrane kod E. viviparus nekako konvergirale po istom modelu kao i mitohondrije“, kaže Angert.
„Imaju visoko presavijenu membranu koja povećava površinu na kojoj ove pumpe za proizvodnju energije mogu da rade, a ta povećana površina stvara elektranu energije.“
Efikasni načini E. viviparus za iskorištavanje hranljivih materija u algama mogli bi imati mnogo koristi u budućnosti. Alge postaju sve popularnije kao izvor obnovljive energije, izvor hrane za stoku, ali i za ljude, jer njihov rast ne ometa poljoprivredu na zemlji.
Ostaju još neke misterije koje treba rešiti. Kako Angert i njegove kolege ističu, potrebno je dalje proučavanje da bi se u potpunosti razumelo kako E. viviparus koristi svoj arsenal enzima. Ali ovo pruža solidnu osnovu za razumevanje njihovih potreba za rastom.
„Smatramo da je izvanredno da su najveće poznate bakterije do sada izbegle izolaciju“, pišu autori. „Ovo sugeriše da su bakterijski behemoti visoko podešeni da prežive u sredinama u kojima su evoluirali.“