G protein-coupled receptors (GPCRs) se nalaze u celom ljudskom telu i uključeni su u mnoge složene signalne puteve. Uprkos njihovoj važnosti u mnogim biološkim procesima, centralni mehanizam spajanja G proteina i povezani prenos signala još uvek nije shvaćen.
Tim istraživača sa Univerziteta u Lajpcigu uspeo je da razume mehanizam prenosa signala preko receptora koji vezuje adrenalin na atomskom nivou. U budućnosti, istraživači će možda moći da koriste ove rezultate kako bi bolje izbegli neželjene efekte pri razvoju lekova.
Studija je objavljena u časopisu Nature Structural & Molecular Biology.
Svaki organizam reaguje na okolinu. Spoljašnji stimulans uzrokuje da telo oslobađa glasnike kao što je adrenalin, koji se vezuju za receptore. Receptori prenose signal drugim proteinima. Ovo pokreće biohemijske kaskade koje dovode do odgovora u organizmu, kao što je reakcija „beži ili se bori“ u slučaju receptora koji vezuje adrenalin.
Lekovi se često modeluju na osnovu ovih glasnika i deluju u interakciji sa receptorima. Neželjeni efekti se mogu javiti ako se lek veže za pogrešan receptor ili ne prenese signal na ispravan intracelularni protein. Da bi to sprečili, naučnici proučavaju kako receptori rade.
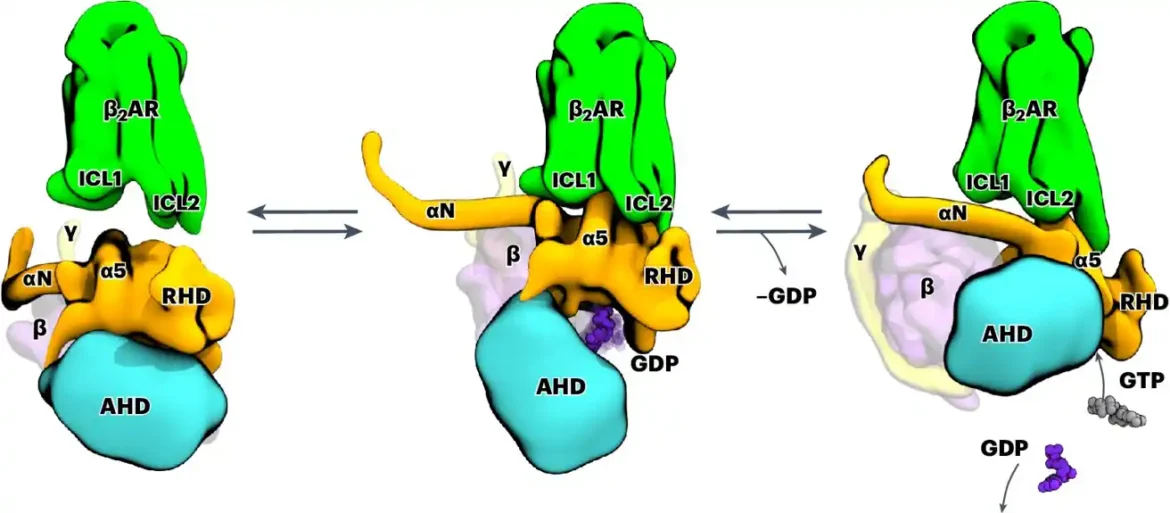
U trenutnoj studiji, profesor Peter Hildebrand i njegov tim sa Instituta za medicinsku fiziku i biofiziku Univerziteta u Lajpcigu pokazuju kako se prenos signala kroz β2 adrenergički receptor odvija na atomskom nivou. Ovo je receptor povezan sa G proteinom (GPCR). Članovi ove superfamilije proteina ugrađeni su u ćelijsku membranu.
Tim je koristio kompjuterski potpomognute simulacije molekularne dinamike, kao i analize biohemijskih i funkcionalnih mutacija za svoja istraživanja. Ovo im je omogućilo da posmatraju kako receptor funkcioniše: vezivanjem, receptor menja trodimenzionalnu strukturu intracelularnog G proteina, koji zatim oslobađa regulatorni molekul GDP.
U sledećem koraku, ovaj G protein se može aktivirati vezivanjem svog stvarnog supstrata GTP i pokrenuti biohemijske kaskade u ćeliji. Tim istraživača je takođe otkrio da tačna funkcija receptora zavisi od rasporeda različitih fleksibilnih strukturnih elemenata. Oni se ne mogu okarakterisati korišćenjem metoda klasične strukturne biologije.
Profesor Hildebrand sada planira da primeni kompjuterski potpomognute biofizičke metode na druge sisteme receptora, kao što je istraživanje gojaznosti, u fokusu medicinskih istraživanja na Univerzitetu u Lajpcigu. „Uporedne studije dinamičke signalizacije su uzbudljive kada se koriste lekovi različitih profila“, objašnjava profesor biofizičkih kompjuterskih simulacija.
Profesor Peter V. Hildebrand istražuje receptore na Medicinskom fakultetu Univerziteta u Lajpcigu od 2017. Od 2008–2014, proučavao je strukturu fotoreceptora rodopsina sa profesorom Klaus-Peterom Hofmannom i dr Patrikom Šererom u Charite-u.
On sada takođe sarađuje sa nobelovcem, profesorom Brajanom Kobilkom i krio-elektronskim mikroskopistom, profesorom Jiorgom Skiniotisom, Univerzitet Stanford, SAD, kako bi bolje razumeli signalizaciju posredovanu GPCR-om. Zajedno su nedavno razjasnili mehanizam vezivanja GTP-a za G protein i njegovu aktivaciju i objavili rezultate u časopisu Nature.
„Prvi put sada imamo sveobuhvatnu sliku o strukturnom mehanizmu signalizacije posredovane receptorima spolja u unutrašnjost ćelije“, kaže Hildebrand. „Ovaj uspeh, pored svojih saradnika, dugujem pre svega talentovanim mladim naučnicima dr Hoseinu Batebiju i dr Giljermu Peresu Ernandezu iz mog tima.“