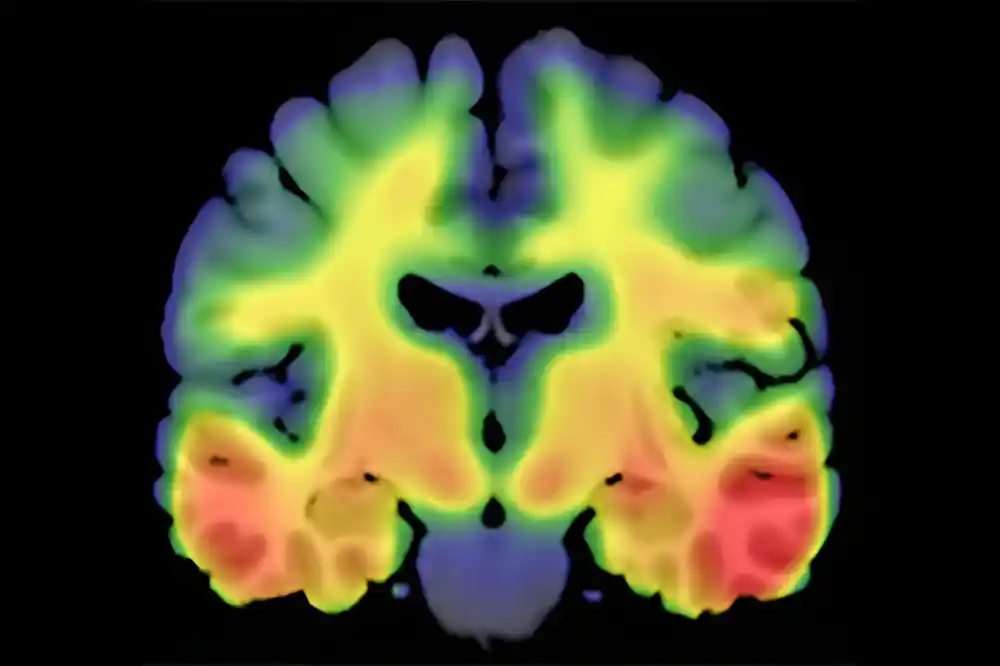
Istraživači Medicinskog fakulteta Univerziteta Indijana identifikovali su novi genetski marker koji bi mogao da igra ulogu u razvoju Alchajmerove bolesti, koju karakterišu dve primarne patologije: amiloid-beta plakovi i neurofibrilarni tau zapleti. Njihovi nalazi, nedavno objavljeni u Nature Communications, mogli bi utrti put za nove terapeutske ciljeve i dijagnostičke alate za bolest.
Studija je uključila međunarodni tim istraživača koji je analizirao genetske i napredne podatke o tau PET imidžingu od više od 3.000 ljudi, što je činilo najvećim naporom do sada u istraživanju genetike kortikalnog taua otkrivenog na PET-u. Identifikovao je genetski lokus – specifičnu lokaciju gena na hromozomu – koji predstavlja značajan deo tau taloženja kod starijih osoba koje imaju ili su u riziku od razvoja Alchajmerove bolesti.
„Identifikovanje ovog novog genetskog markera otvara novi put za istraživanje i potencijalni terapijski razvoj ciljanjem na abnormalni oblik tau proteina koji se sastoji od čvorova koji se vide u mozgu kod Alchajmerove bolesti“, rekao je Andrev J. Saikin, psihijatar, glavni istraživač studije. i Raimond C. Beeler, profesor radiologije na Medicinskom fakultetu IU.
„Dok su mnoge prethodne studije asocijacije koje obuhvataju čitav genom upoređivale genetske profile pacijenata sa Alchajmerovom bolešću sa kognitivno neoštećenim starijim odraslim osobama, ova studija je koristila tau PET skeniranje kao kontinuirani fenotip za otkrivanje genetskog lokusa koji čini značajan deo tau depozicije kod učesnika studije.“
Saikin, koji takođe vodi školski centar za istraživanje Alchajmerove bolesti Indijane i IU centar za neuroimaging, rekao je da su prethodne studije napravile napredak u identifikaciji genetskih varijanti povezanih sa taloženjem amiloida, da je razumevanje genetskih pokretača tau depozicije bilo mnogo izazovnije zbog nedostatka velikih skupova podataka sa tau PET i genetskim informacijama.
Ova studija popunjava taj jaz, pokazujući da je varijanta rs2113389 koja se nalazi na hromozomu 2p22.2, između gena CIP1B1 i RMDN2, snažno povezana sa povećanim opterećenjem tau u više regiona mozga. Sama ova varijanta objasnila je približno 4,3% varijacije tau depozicije, nadmašujući čak i doprinos široko poznatog APOE4 gena, koji čini 3,6%.
„Potrebna su dalja istraživanja da bi se izvuklo i utvrdilo šta tačno pokreće ovo udruženje“, rekao je Sajkin. „Sada imamo novi lokus na preseku ovih gena za proučavanje kao potencijalne mete za dijagnostičke i terapijske pristupe.“
Proučavanih 3.000 učesnika bilo je sa 12 različitih lokacija širom sveta. Neki od pojedinaca nisu imali nikakvo kognitivno oštećenje, dok su drugi imali blago ili teško kognitivno oštećenje.
„Moramo da ponovimo nalaze u većim uzorcima,“ rekla je Shannon L. Risacher, Ph.D., glavni istraživač studije i vanredni profesor radiologije na Medicinskom fakultetu IU. „Većina ispitivanih kohorti pacijenata nalazi se u Sjedinjenim Državama, Kanadi i Australiji, ali PET skeniranje se sprovodi u mnogim drugim delovima sveta. Budući cilj bi bio da se proširi veličina uzorka kako bi se replicirali naši rezultati.“
Tim takođe planira da nastavi proučavanje lokusa i njegovog ponašanja u modelima miša.
„Veoma važan korak koji prati ljudska otkrića je funkcionalnija validacija u modelskim sistemima, uključujući miševe i ćelijske kulture ili organoide“, rekao je dr Kvangsik Nho, glavni istraživač studije i profesor radiologije na IU školi Lek. „Želimo da vidimo da li se ovaj efekat može modelirati u laboratoriji, što bi u velikoj meri moglo olakšati napore za razvoj lekova.“
Sajkin je rekao da je kombinovanje naprednog neuroimaginga i genetike nešto što istraživački tim teži već dugi niz godina.
„Uzbudljivo je videti kako ovaj pristup donosi novu potencijalnu metu“, rekao je Sajkin. „Da bismo na kraju sprečili Alchajmerovu bolest, moramo bolje razumeti šta pokreće plakove i zamršenost na prvom mestu. Genetska istraživanja zajedno sa biomarkerima i kognitivnim studijama omogućiće ranije otkrivanje i preciznije intervencije kod onih koji su pogođeni ili pod povećanim rizikom.“