Protein nazvan Meteorin-like (METRNL) u mikrookruženju tumora troši energiju iz T ćelija, čime ozbiljno ograničava njihovu sposobnost da se bore protiv raka, prema novom istraživanju koje su režirali istraživači sa Medicinskog fakulteta Univerziteta Džon Hopkins i Centra za rak Džons Hopkins Kimel. i njegov Bloomberg-Kimmel institut za imunoterapiju raka.
Pronalaženje načina da se blokiraju efekti METRNL signalizacije na T ćelije koje infiltriraju tumor može omogućiti ovim imunim ćelijama da povrate energiju neophodnu za eliminaciju tumora.
Izveštaj o radu objavljen je 6. avgusta u časopisu Imunitet.
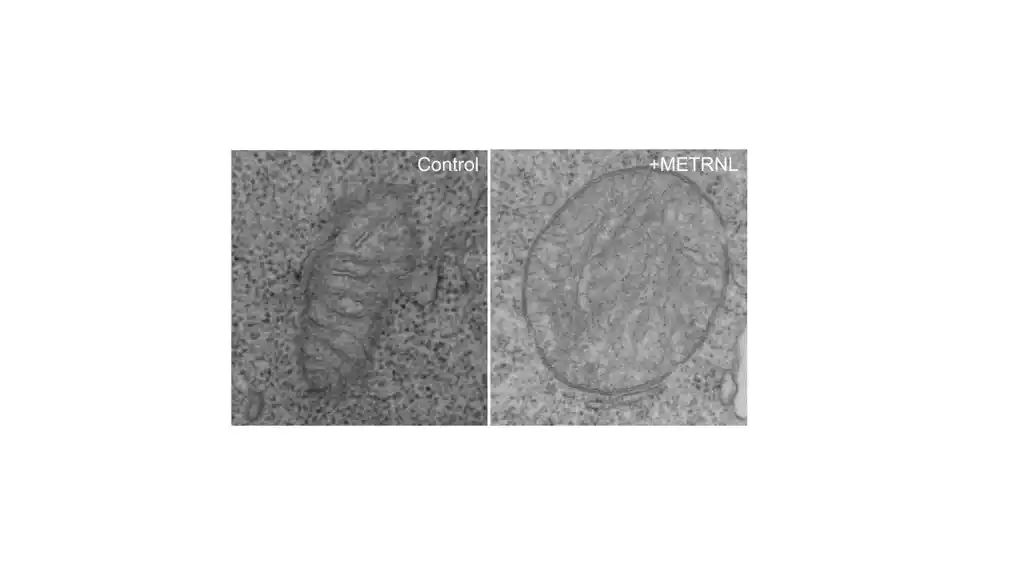
METRNL je ranije opisan u medicinskoj literaturi — u početku je igrao ulogu u održavanju hladnoće ili zagrevanju životinja (i ljudi) tako što probija rupe u mitohondrijama (fabrika energije) masnih ćelija kako bi one proizvodile toplotu. Međutim, ranije nije bilo poznato da je aktivan u raku ili u T ćelijama, kaže glavni autor studije Christopher Jackson, MD, docent neurohirurgije na Johns Hopkinsu.
Kada T ćelije pokušavaju da eliminišu tumor, stanje hronične stimulacije/stresa dovodi do toga da luče METRNL, objašnjava Džekson. Jednom kada se METRNL izluči, on stupa u interakciju sa mitohondrijama i probija rupe u lancu transporta elektrona, klaster proteina koji učestvuje u procesu stvaranja energije.
Kada T ćelije više ne mogu da prate svoje energetske potrebe, one prestaju da pokušavaju da ubiju ćelije raka, što omogućava ćelijama raka da se umnožavaju i šire.
„Drugi su pokazali da metabolička disfunkcija ograničava sposobnost T ćelija da se bore protiv raka, ali mi smo među prvima koji su opisali diskretni signalni put koji uzrokuje da se to dogodi“, kaže Džekson.
„Većina prethodnog rada je razmatrala kako nedostatak specifičnih hranljivih materija u tumorima ograničava sposobnost T ćelija da funkcionišu. Problem je što je ovo teško modifikovati jer je teško uneti prave hranljive materije u tumor i usmeriti ih do T ćelija. .
„Potencijalno možemo učiniti mnogo bolje ciljanjem signalnog puta jer ga možemo blokirati ili uključiti ili isključiti, ali do sada niko nije identifikovao takav put koji obnavlja metaboličko zdravlje T ćelija u tumorima.“
U nizu laboratorijskih istraživanja, istraživači su prvo proučavali T ćelije iz tumorskog tkiva i krvi pacijenata sa prethodno nelečenim tumorima mozga (glioblastoma), karcinomom prostate, karcinomom mokraćne bešike i karcinomom bubrežnih ćelija/bubrega i izvršili sekvenciranje RNK da bi pokušali da identifikuju gene. odgovoran za disfunkciju u tumoru. METRNL je bio gen sa najvećom ekspresijom.
Zatim su želeli da saznaju šta čini T ćelije da luče METRNL na prvom mestu, otkrivši da je razlog hronična stimulacija. Normalno, imuni sistem se aktivira kada je stimulisan da se bori protiv infekcije, a zatim se smanjuje kada se ta bolest povuče. Ali u okruženju raka, T ćelije su hronično stimulisane, što uzrokuje da postanu nefunkcionalne.
Takođe je otkriveno da METRNL luče druge imune ćelije u tumorima kao što su makrofagi i dendritične ćelije, ali deluje specifično na T ćelije.
Dodatna istraživanja su utvrdila da METRNL deluje direktno na mitohondrije i razdvaja lanac transporta elektrona. Kako T ćelije gube energiju i počinju da propadaju, one povećavaju svoje pokušaje da iskoriste glukozu (prirodni šećer) kao rezervni izvor energije.
Ali, pošto je u okruženju tumora malo glukoze, oni nastavljaju da skapaju i na kraju umiru. Ovo je jedan od načina na koji tumori mogu nastaviti da rastu. Brisanje METRNL-a u modelima različitih tipova raka u istraživanjima istraživača univerzalno je odložilo rast tumora.
Konačno, istraživači su primetili da se METRNL aktivira preko familije transkripcionih faktora (proteina koji kontrolišu brzinu transkripcije genetskih informacija sa DNK na RNK) nazvanih E2F, da zavisi od signalizacije od strane receptora zvanog PPAR delta, i da modulira ove faktori nizvodno mogu blokirati efekte METRNL.
Sledeći koraci su da se utvrdi kako ovo može pomoći pacijentima, kaže Džekson. On i njegove kolege aktivno rade na različitim sredstvima za ciljanje METRNL-E2F-PPAR delta puta ili da kombinuju ciljani tretman sa drugim imunoterapijama.
„Smatramo da je jedan od razloga zašto neke trenutne imunoterapije ne uspevaju to što zahtevaju više energije od imunih ćelija koje već funkcionišu sa smanjenim kapacitetom“, kaže on. „Blokiranje puta može omogućiti da ove imunoterapije koje možda nisu bile efikasne u prošlosti budu efikasnije jer će biti dovoljno goriva za T ćelije da zadovolje tu povećanu potražnju.“