Alchajmerova bolest (AD) ostaje jedan od najizazovnijih i najrasprostranjenijih neurodegenerativnih poremećaja, koji pogađa milione pojedinaca širom sveta. U novoj studiji objavljenoj u Developmental Cell, istraživači iz laboratorije Vim Annaert (VIB-KU Leuven) identifikovali su novi mehanizam potencijalno povezan sa ranim fazama AD. Oni su pokazali da fragment amiloidnog prekursora proteina (APP), nazvan APP-CTF, remeti komunikaciju između ćelijskih odeljaka koji su ključni za skladištenje kalcijuma i odlaganje otpada, što bi mogao biti rani događaj koji prethodi smrti neuronske ćelije.
Ovi nalazi, sa potencijalnim implikacijama za razvoj novih tretmana AD, sugerišu da sprečavanje akumulacije APP-CTF-a treba uzeti u obzir kako bi se razvili efikasniji tretmani.
Alchajmerovu bolest karakteriše progresivni gubitak kognitivnih funkcija, oštećenje pamćenja i promene ponašanja. Jedna od vidljivih karakteristika u mozgu ljudi sa Alchajmerovom bolešću je formiranje amiloidnih plakova — nakupina β-amiloidnih (Aβ) peptida, koji su degradirani proizvodi amiloidnog prekursora proteina (APP). Ovi Aβ-fragmenti se akumuliraju u neuronima u ranoj fazi bolesti, čak i pre nego što se primeti kognitivni pad.
Novo istraživanje, međutim, sugeriše da bi se možda čak i dešavali raniji događaji u mozgu AD pre formiranja plaka i da APP protein igra ulogu u ovim ranim fazama. Mehanizam iza ovoga ostao je misterija do sada.
U svojoj najnovijoj studiji, laboratorija Annaert u VIB-KU Leuven centru za istraživanje mozga i bolesti identifikovala je mehanizam koji objašnjava kako APP može doprineti ovim ranim fazama AD. Ovo otkriće bi moglo dovesti do novog pravca u istraživanju i pristupima lečenja AD.
APP se nalazi u ćelijskim membranama moždanih ćelija. Mozak stalno proizvodi nove APP molekule dok razgrađuje i uklanja stare. Ovaj proces uključuje enzimske makaze, pri čemu je gama-sekretaza poslednja koja generiše dobro poznate i dobro proučavane Aβ peptide u AD.
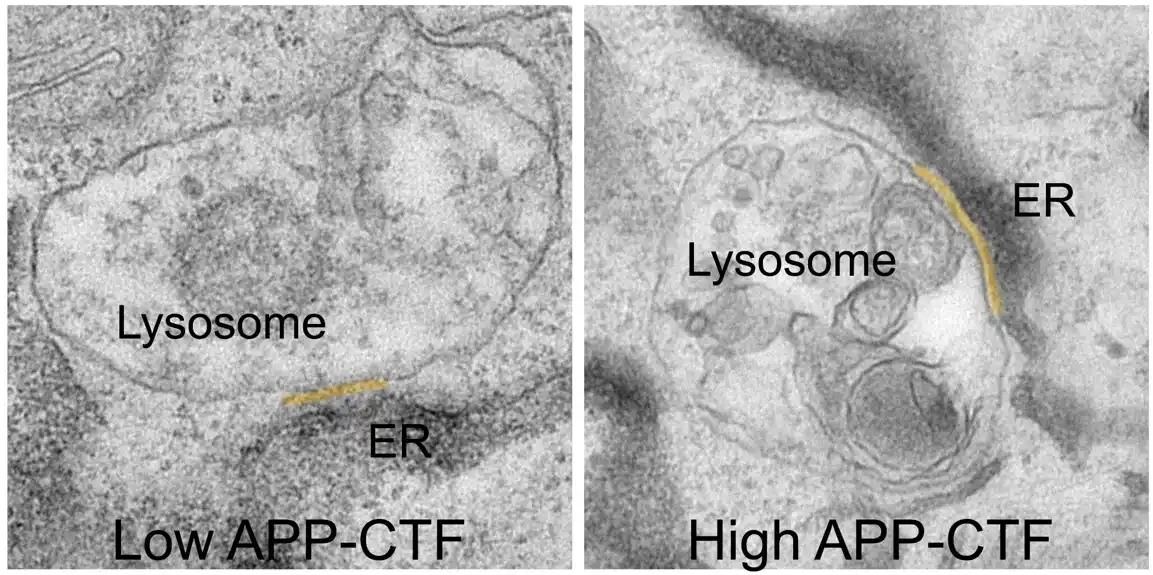
Dugo vremena se smatralo da bi blokiranje gama-sekretaze bilo logičan korak da se spreči proizvodnja toksičnih Aβ fragmenata. Međutim, ovo dovodi do akumulacije njihovog prekursora, APP-C-terminalnih fragmenata, ili APP-CTF-ova. Sada su istraživači otkrili da su ovi fragmenti toksični i za neurone. Izgleda da se akumuliraju između endoplazmatskog retikuluma (ER), odeljka koji je ključan za sintezu lipida i skladištenje kalcijuma, i lizozoma, takozvanih „kanti za otpad“ neurona, koji su kritični za razgradnju otpadnih proizvoda ćelije.
„Na taj način, APP-CTF-ovi narušavaju delikatnu ravnotežu kalcijuma unutar lizozoma“, objašnjava dr Marine Bretu, prvi autor studije. „Ovaj poremećaj pokreće kaskadu događaja. ER više ne može efikasno da dopuni lizozome kalcijumom, što dovodi do nakupljanja holesterola i smanjenja njihove sposobnosti da razgrađuju ćelijski otpad. Ovo rezultira kolapsom celog endolizozomalnog sistema, a ključni put za održavanje zdravih neurona.“
Nova studija dalje podržava da APP-CTF-ovi koji nastaju supresijom gama-sekretaze mogu zapravo biti krivac za endolizosomalnu disfunkciju, kao što je primećeno u vrlo ranim fazama AD.
Ovo istraživanje značajno unapređuje naše razumevanje potencijalnih uzroka bolesti u ranim fazama AD. Izvanredan rezultat ove studije je da ove rane faze mogu biti uzrokovane drugim fragmentom istog APP molekula, a ne Aβ.
Ovo ima značajne implikacije za trenutne terapijske pristupe koji imaju za cilj da očiste AD mozak od amiloidnih plakova, pošto oni imaju tendenciju da ignorišu toksične efekte drugih fragmenata. Drugi pokušaji se fokusiraju na tau proteine ili neuroinflamaciju, što su druga obeležja progresije AD koji ciljaju na kasnije događaje. Međutim, rana intervencija je verovatno ključ za zaustavljanje ili čak prevenciju AD.
„Neuspeh kliničkih ispitivanja sa inhibitorima gama-sekretaze može se objasniti činjenicom da smo se fokusirali na samo jednog krivca i to u prekasnoj fazi bolesti“, objašnjava prof. Annaert, viši autor studije.
„Naši rezultati istraživanja sugerišu da modulatori gama-sekretaze, koji mogu pomoći u promociji uklanjanja toksičnih APP-CTF-a bez potpunog blokiranja enzima, mogu biti relevantnija meta za ranu intervenciju u AD. Ključ bi mogao biti pronalaženje prave ravnoteže između APP-a. CTF čišćenje i prevencija plaka.“
Gledajući unapred, naučnici udružuju napore sa kolegama da razviju ove modulatore na osnovu ovih novih uvida i nastaviće da istražuju ćelijsku homeostazu u ranim fazama AD.