Blokiranje formiranja filamenata – struktura sa više enzima koje podstiču aktivnost raka – može ponuditi nove načine za kontrolu proliferacije ćelija raka, prema novoj studiji koju su vodili istraživači iz Kornela.
Glutaminaze, enzimi koji formiraju ove filamente, pomažu u transformaciji glutamina u glutamat, koji pokreće duži niz reakcija koje proizvode energiju za rast ćelija raka.
„Glutaminaze su važne za preživljavanje ćelija raka, ali takođe obezbeđuju neophodne građevne blokove koji im omogućavaju da se izvuku iz tumora i metastaziraju“, rekao je Richard Cerione, uvaženi profesor umetnosti i nauke na Odeljenju za hemiju i hemijsku biologiju ( College of Arts and Sciences), i profesor na Odseku za molekularnu medicinu (Koledž veterinarske medicine), koji je vodio studiju, objavljenu u Nature Communications. Koautori su doktoranti Ši Feng, Kodi Aplin i Tien Ngujen i naučni saradnik Šon Milano.
Oslanjanje ćelija raka na glutamin i njegove nizvodne proizvode je toliko važno da naučnici nazivaju ćelije raka „zavisnim od glutamina“. Iskorišćavanje ove zavisnosti od glutamina postalo je važna strategija za razvoj lekova protiv raka, sa metaboličkim putem glutamina kao primarnom metom.
Aktivnost glutaminaze je obično niska u normalnim zdravim ćelijama, ali postaje veoma aktivna u ćelijama raka. Šta pokreće tako visoku enzimsku aktivnost ostalo je nejasno. „Želeli smo da razumemo kako ovi enzimi postaju tako aktivni“, rekao je Cerione.
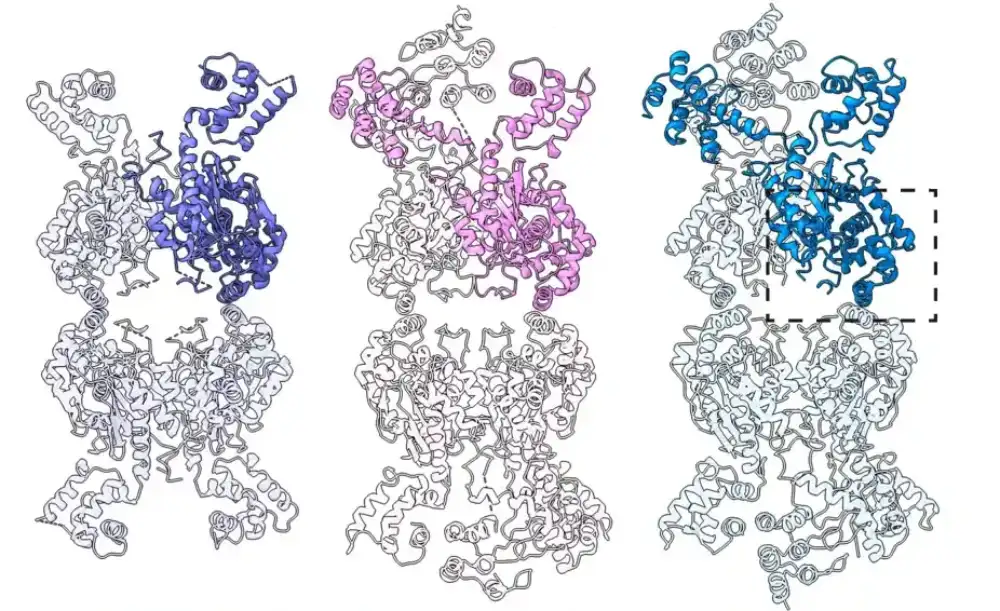
U normalnim ćelijama, enzimi se vezuju u parove, koji se takođe nazivaju dimeri; u ćelijama raka, međutim, ovi enzimi se okupljaju u parove dimera, formirajući grupe od četiri ili tetramera. Iz drugih eksperimenata, Cerione je imao neke indikacije da su ovi tetrameri tada prerasli u izdužene strukture, nazvane filamenti, ali njihova uloga nije bila jasna.
Cerione i njegov tim okrenuli su se krioelektronskoj mikroskopiji (crioEM), tehnologiji vizuelizacije gde se uzorci zamrzavaju i posmatraju pod elektronskim mikroskopom, koji proizvodi slike strukture proteina visoke rezolucije.
Prilikom ispitivanja enzima glutaminaze pod katalitičkim uslovima korišćenjem crioEM-a, Cerionov tim je potvrdio svoja prethodna zapažanja: Kada su ovi enzimi aktivni, tetrameri se spajaju i formiraju filamente dužine do 30 tetramera. „Onda smo pitali, zašto su nam potrebni ti filamenti?“ rekao je.
Ispostavilo se da ovi filamenti značajno pojačavaju aktivnost glutaminaza. Kada je tim dodao jedinjenja koja blokiraju formiranje filamenata, enzimi su prestali da transformišu glutamin u glutamat, čime su ćelije raka izgladnjile u snabdevanju hranljivim materijama. Tim je pokazao ovaj rezultat i u ćelijskim kulturama i na njihovim modelima miša.
Cerione misli da ovi glutaminazni filamenti mogu funkcionisati „kao skela koja sastavlja velike metaboličke komplekse“, što znači da ne samo da pretvaraju glutamin u glutamat, već i omogućavaju sledećim enzimima u lancu reakcija da se pričvrste na filament i pretvaraju glutamat u sledeći proizvod .
„Ovo bi se nastavilo sve dok je glutamin dostupan glutaminazi“, rekao je Cerione. „Kada se sav ovaj supstrat potroši, filamenti glutaminaze se ponovo razdvajaju na svoje pojedinačne tetramerne jedinice. Proces zatim počinje ponovo kada postane dostupno više glutamina.“
Za sledeće korake, Cerione želi da fino podesi svoje razumevanje kako da isključi formiranje filamenata, eksperimentišući sa novim jedinjenjima i rafinišući postojeća. Paralelno sa tim, dodatno istraživanje formiranja filamenta omogućiće preciznije saznanje o tome gde da se blokiraju filamenti i na kraju omogući bolji dizajn leka.
„Razumevanje kako blokirati formiranje filamenta moglo bi da ima ogroman uticaj“, rekao je on, „jer je visoka zavisnost od glutamina od suštinskog značaja za zadovoljavanje strogih metaboličkih zahteva i za rast i opstanak različitih ćelija raka, uključujući male ćelija raka pluća, raka dojke i ćelija tumora mozga.“