Mali uređaj koji su napravili naučnici sa MIT-a i Singapur-MIT Alijanse za istraživanje i tehnologiju mogao bi da se koristi za poboljšanje bezbednosti i efikasnosti tretmana ćelijskom terapijom za pacijente koji pate od povreda kičmene moždine.
U ćelijskoj terapiji, kliničari stvaraju ono što je poznato kao indukovane pluripotentne matične ćelije reprogramiranjem nekih ćelija kože ili krvnih zrnaca uzetih od pacijenta. Da bi lečili povredu kičmene moždine, oni bi naterali ove pluripotentne matične ćelije da postanu progenitorne ćelije, koje su predodređene da se diferenciraju u ćelije kičmene moždine. Ovi progenitori se zatim transplantiraju nazad u pacijenta.
Ove nove ćelije mogu da regenerišu deo povređene kičmene moždine. Međutim, pluripotentne matične ćelije koje se ne menjaju u potpunosti u progenitore mogu formirati tumore.
Ovaj istraživački tim je razvio mikrofluidni ćelijski sorter koji može ukloniti oko polovine nediferenciranih ćelija – onih koje potencijalno mogu postati tumori – u seriji, bez izazivanja bilo kakvog oštećenja potpuno formiranih progenitorskih ćelija.
Uređaj visoke propusnosti, koji ne zahteva posebne hemikalije, može sortirati više od 3 miliona ćelija u minuti. Pored toga, istraživači su pokazali da povezivanje mnogih uređaja zajedno može sortirati više od 500 miliona ćelija u minuti, što ovo čini održivijim metodom da se jednog dana poboljša bezbednost tretmana ćelijske terapije.
Osim toga, plastični čip koji sadrži mikrofluidni sorter ćelija može se masovno proizvoditi u fabrici po veoma niskoj ceni, tako da bi uređaj bio lakši za implementaciju u velikim razmerama.
„Čak i ako imate ćelijsku terapiju koja spašava živote koja čini čuda za pacijente, ako ne možete da je proizvedete isplativo, pouzdano i bezbedno, onda bi njen uticaj mogao biti ograničen. Naš tim je strastven u vezi sa tim problemom – želimo da učinite ove terapije pouzdanijim i lako dostupnim“, kaže Džongjoon Han.
Han je profesor elektrotehnike i računarstva i biološkog inženjerstva na MIT-u, član Istraživačke laboratorije za elektroniku (RLE) i ko-vodeći glavni istraživač istraživačke grupe CAMP (Kritička analitika za proizvodnju personalizovane medicine) u Singapuru -MIT Alijansa za istraživanje i tehnologiju (SMART).
Hanu se u radu pridružuje ko-stariji autor Sing Iian Chev, profesor hemije, hemijskog inženjerstva i biotehnologije na Medicinskom fakultetu Lee Kong Chian i nauke o materijalima i inženjeringu na tehnološkom univerzitetu Naniang u Singapuru i glavni istraživač CAMP-a; ko-vodeći autori Tan Dai Nguien, CAMP istraživač; Vai Hon Chooi, viši naučni saradnik u Singapurskoj agenciji za nauku, tehnologiju i istraživanje (A*STAR); i Hiungkook Jeon, postdoc MIT; kao i drugi u NTU i A*STAR.
Istraživanje je objavljeno danas (7. februara) u časopisu Translaciona medicina matičnih ćelija.
Rizik od raka koji predstavljaju nediferencirane indukovane pluripotentne matične ćelije ostaje jedan od najhitnijih izazova u ovoj vrsti ćelijske terapije.
„Čak i ako imate veoma malu populaciju ćelija koje nisu u potpunosti diferencirane, one bi se i dalje mogle pretvoriti u ćelije slične raku“, dodaje Han.
Kliničari i istraživači često nastoje da identifikuju i uklone ove ćelije tražeći određene markere na njihovim površinama, ali do sada istraživači nisu uspeli da pronađu marker koji je specifičan za ove nediferencirane ćelije. Druge metode koriste hemikalije za selektivno uništavanje ovih ćelija, ali tehnike hemijskog tretmana mogu biti štetne za diferencirane ćelije.
Mikrofluidni sorter visoke propusnosti, koji može sortirati ćelije na osnovu veličine, prethodno je razvio CAMP tim nakon više od decenije rada. Ranije je korišćen za sortiranje imunih ćelija i mezenhimalnih stromalnih ćelija (druga vrsta matičnih ćelija), a sada tim proširuje svoju upotrebu na druge tipove matičnih ćelija, kao što su indukovane pluripotentne matične ćelije, kaže Han.
„Zainteresovani smo za regenerativne strategije za poboljšanje popravke tkiva nakon povreda kičmene moždine, jer ova stanja dovode do razornog funkcionalnog oštećenja. Nažalost, trenutno ne postoji efikasan pristup regenerativnom lečenju povreda kičmene moždine“, kaže Chu.
„Progenitorske ćelije kičmene moždine izvedene iz pluripotentnih matičnih ćelija imaju veliko obećanje, jer mogu da generišu sve tipove ćelija koje se nalaze unutar kičmene moždine kako bi obnovile strukturu i funkciju tkiva. Da bismo mogli efikasno da iskoriste ove ćelije, prvi korak bi bio da se obezbedi njihovo bezbednost, što je cilj našeg rada“.
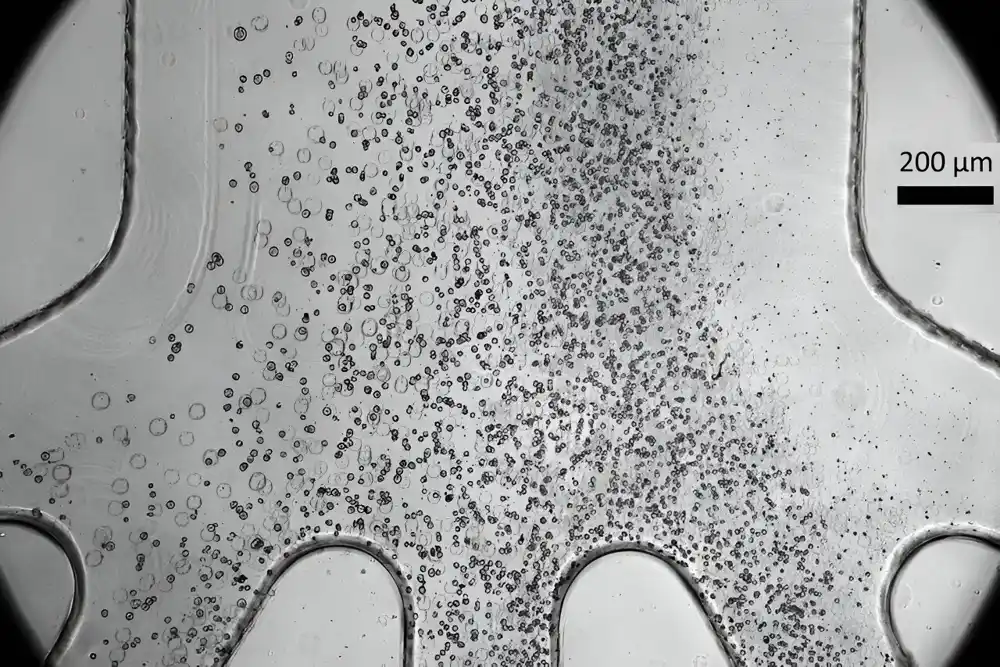
Tim je otkrio da pluripotentne matične ćelije imaju tendenciju da budu veće od progenitora koji potiču od njih. Pretpostavlja se da pre nego što se pluripotentna matična ćelija diferencira, njeno jezgro sadrži veliki broj gena koji nisu isključeni ili potisnuti. Kako se diferencira za određenu funkciju, ćelija potiskuje mnoge gene koji joj više neće biti potrebni, značajno smanjujući jezgro.
Mikrofluidni uređaj koristi ovu razliku u veličini za sortiranje ćelija.