Neki nasledni genetski defekti izazivaju preterani imuni odgovor koji može biti fatalan. Koristeći alat za uređivanje gena CRISPR-Cas9, takvi defekti se mogu ispraviti, čime se normalizuje imuni odgovor, kako istraživači predvođeni Klausom Rajevskim iz Centra Maks Delbrik sada izveštavaju u Naučna imunologija.
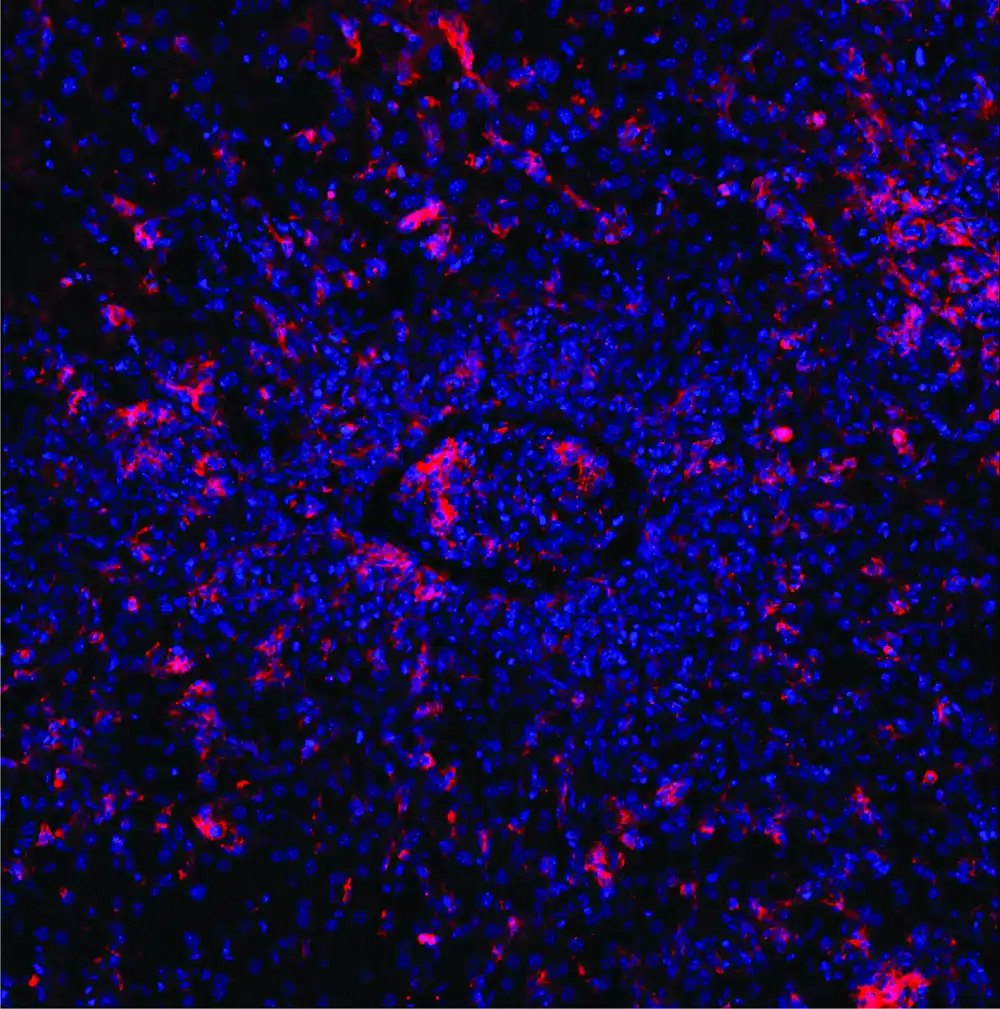
Porodična hemofagocitna limfohistiocitoza (FHL) je retka bolest imunog sistema koja se obično javlja kod odojčadi i male dece mlađe od 18 meseci. Stanje je teško i ima visoku stopu smrtnosti. Uzrokuju ga različite genske mutacije koje sprečavaju normalno funkcionisanje citotoksičnih T ćelija. Ovo su grupe imunih ćelija koje ubijaju ćelije zaražene virusom ili na drugi način izmenjene ćelije.
Ako se dete sa FHL zarazi virusom – kao što je Epstein-Barr virus (EBV), ali i drugim virusima – citotoksične T ćelije ne mogu eliminisati zaražene ćelije. Umesto toga, imuni odgovor izmiče kontroli. To dovodi do citokinske oluje i prekomerne inflamatorne reakcije koja utiče na ceo organizam.
„Lekari leče FHL kombinacijom hemoterapije, imunosupresije i transplantacije koštane srži, ali mnoga deca i dalje umiru od bolesti“, kaže profesor Klaus Rajevski, koji vodi laboratoriju za imunološku regulaciju i rak u Centru Maks Delbrik.
On i njegov tim su stoga razvili novu terapijsku strategiju. Koristeći alat za uređivanje gena CRISPR-Cas9, istraživači su uspeli da poprave defektne T ćelije kod miševa i od dve kritično bolesne bebe. Popravljene citotoksične T ćelije su tada funkcionisale normalno, a miševi su se oporavili od hemofagocitne limfohistiocitoze.
Polazna tačka za studiju bili su miševi kod kojih je tim mogao da oponaša EBV infekcije. Kod ovih životinja, istraživači su promenili gen nazvan perforin tako da je njegova funkcija potpuno izgubljena ili ozbiljno ugrožena – uobičajeni genetski defekt kod pacijenata sa FHL.
Kada su potom izazvali stanje koje liči na EBV infekciju, zahvaćene B ćelije su se nekontrolisano umnožavale jer defektne citotoksične T ćelije nisu bile u stanju da ih eliminišu. Kao rezultat toga, imuni odgovor je postao prekomeran i miševi su razvili hemofagocitnu limfohistiocitozu.
Tim je zatim sakupio T memorijske matične ćelije – to jest, dugovečne T ćelije iz kojih aktivne citotoksične T ćelije mogu sazreti – iz krvi miševa. Istraživači su koristili alat za uređivanje gena CRISPR-Cas9 da poprave defektni gen za perforin u memorijskim T ćelijama, a zatim ubrizgali ispravljene ćelije nazad u miševe. Imuni odgovor kod životinja se smirio i njihovi simptomi su nestali.
Prvi autor rada, dr Ksun Li, koristio je uzorke krvi dve bolesne bebe da bi testirao da li strategija funkcioniše i kod ljudi. Jedan je imao defektan gen za perforin, a drugi drugi defektni gen.
„Naša tehnika popravke gena je preciznija od prethodnih metoda, a T ćelije su praktično nepromenjene nakon uređivanja gena“, kaže Li. „Takođe je bilo fascinantno videti koliko efikasno T ćelije memorije mogu da se umnože i poprave čak i iz male količine krvi.“