Istraživanje Univerziteta u Bafalu je identifikovalo kako pogrešan korak u nastanku ključne komponente bubrega uzrokuje infantilnu cistinozu, retku bolest koja značajno skraćuje životni vek pacijenata.
Objavljen 30. novembra u Međunarodnom časopisu za molekularne nauke, rad otkriva da se mehanizmi koji uzrokuju bolest mogu rešiti i potencijalno izlečiti pomoću tehnike za uređivanje genoma CRISPR. To bi moglo učiniti nepotrebnim transplantaciju bubrega, najefikasniji tretman koji je trenutno dostupan za ove pacijente.
Infantilna cistinoza, najčešća i najteža vrsta cistinoze, nastaje kao rezultat akumulacije cistina, aminokiseline u ćelijama tela. Nagomilavanje oštećuje ćelije u celom telu, posebno bubrege i oči. Lečenje se sastoji od lekova koji deluju na snižavanje nivoa cistina u telu, kao i od terapija koje se bave poremećenim rastom ove dece zbog nemogućnosti da pravilno apsorbuju hranljive materije. Neka deca zahtevaju cevi za hranjenje. Na kraju, pacijentima sa infantilnom cistinozom, koja se naziva i nefropatska cistinoza, biće potrebna dijaliza i transplantacija bubrega.
Pluripotentne matične ćelije izazvane ljudima (hiPSC) su matične ćelije koje se mogu diferencirati u mnogo različitih tipova ćelija. Oni imaju ogroman potencijal za proučavanje genetskih bolesti; nedostatak je bio u tome što je diferencijacija u određene tipove ćelija bila problematična. Takav je slučaj sa mnogim tipovima ćelija koje se nalaze u bubrezima.
Ali novi protokol koji je razvio ovaj istraživački tim bio je uspešan.
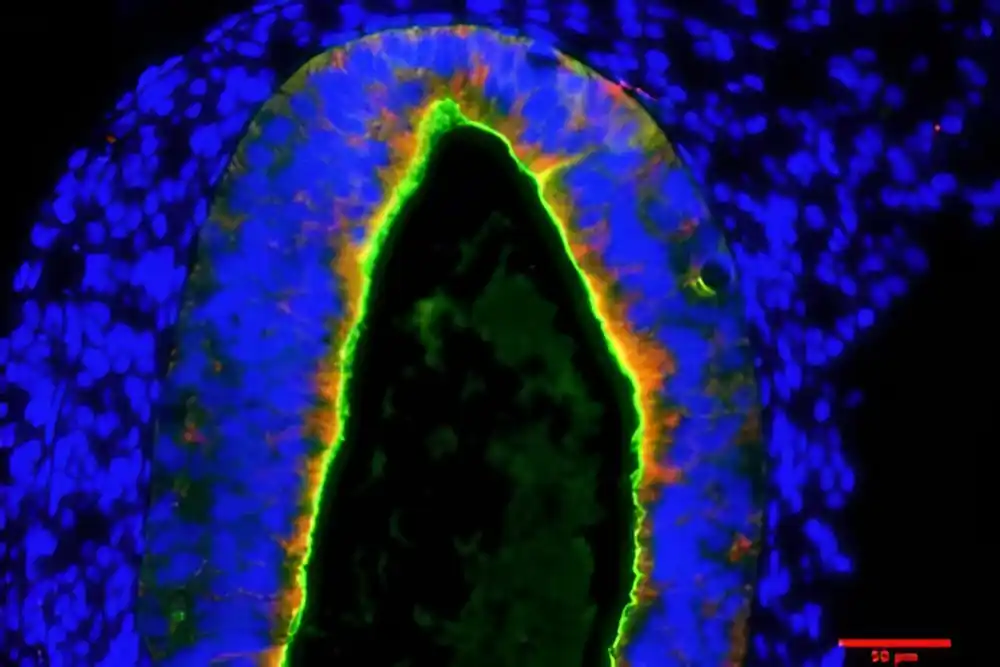
„Kada su naše normalne pluripotentne matične ćelije izazvane ljudima bile podvrgnute protokolu diferencijacije koji smo razvili, uspeli smo da pokažemo ekstenzivnu ekspresiju fiziološki važnih markera proksimalnog tubula bubrega, specifičnog segmenta nefrona koji je promenjen u ovoj bolesti“, kaže Meri. L. Taub, Ph.D., viši autor rada i profesor biohemije na Jacobs School of Medicine and Biomedical Sciences na UB.
Ramkumar Thiiagarajan, Ph.D., docent gerijatrijskih studija na Univerzitetu u Kanzasu i bivši postdoktorski saradnik na UB, prvi je autor rada.
Protokol je uključivao ekstrakciju matičnih ćelija iz zdrave osobe i osobe sa infantilnom cistinozom. Istraživači su razvili medijum za uzgoj matičnih ćelija koji je uključivao mali broj definisanih komponenti prisutnih u krvi, uključujući insulin, specifične proteine, faktore rasta i druge. „Sprovođenje protokola diferencijacije pod ovim uslovima dogodilo se blagovremeno“, kaže Taub, „nismo morali da čekamo nedeljama zaredom, i to se dogodilo na ponovljiv način“.
Istraživači su uspeli da efikasno diferenciraju hiPSC u proksimalni tubul bubrega, tip nefrona u bubregu koji je oštećen kod infantilne cistinoze, kao i kod drugih bolesti bubrega.
„Za razliku od drugih studija, uspeli smo da zadržimo brojne markere u tubulu koji su fiziološki važni u reapsorptivnim funkcijama bubrega“, kaže Taub. „Iako su ovi markeri izraženi i u normalnim i u hiPSC-ovima izvedenim iz cistinoze, geneza tubula je poremećena u ćelijama izvedenim iz cistinoze, oponašajući ono što se dešava kod infantilne cistinoze.“
Taj nalaz znači da bi se tehnika za uređivanje genoma CRISPR mogla koristiti za popravku defektnog genoma i potencijalno izlečenje bolesti. „Normalni gen se može uvesti u genom cistinotičnih hiPSC-a, koji se zatim mogu ubrizgati u bubreg da bi se zamenili defektni proksimalni tubuli pojedinaca sa infantilnom cistinozom“, kaže Taub.
„Kod cistinotičnih pojedinaca, proksimalni tubul bubrega degeneriše, verovatno zbog programirane ćelijske smrti“, objašnjava Taub, „tako da ne bi trebalo zameniti ceo bubreg. Defektni proksimalni tubuli bubrega kod osoba sa ovom bolešću mogu se zameniti sa normalnim tubulima nakon uvođenja normalnog gena u cistinotične hiPSC dobijene od pacijenta. I pošto su ovi tubuli iz ćelija dobijenih od pacijenta, ne bi trebalo da postoji problem sa odbacivanjem tkiva.“
Nalazi su primenljivi na druge bolesti bubrega gde je oštećen proksimalni tubul bubrega, uključujući akutnu povredu bubrega koja može dovesti do hronične bolesti bubrega i bubrežne insuficijencije, a može biti i fatalna.
Inicijalne studije će morati da se sprovedu sa životinjskim modelima kao i sa ćelijama kulture tkiva in vitro.