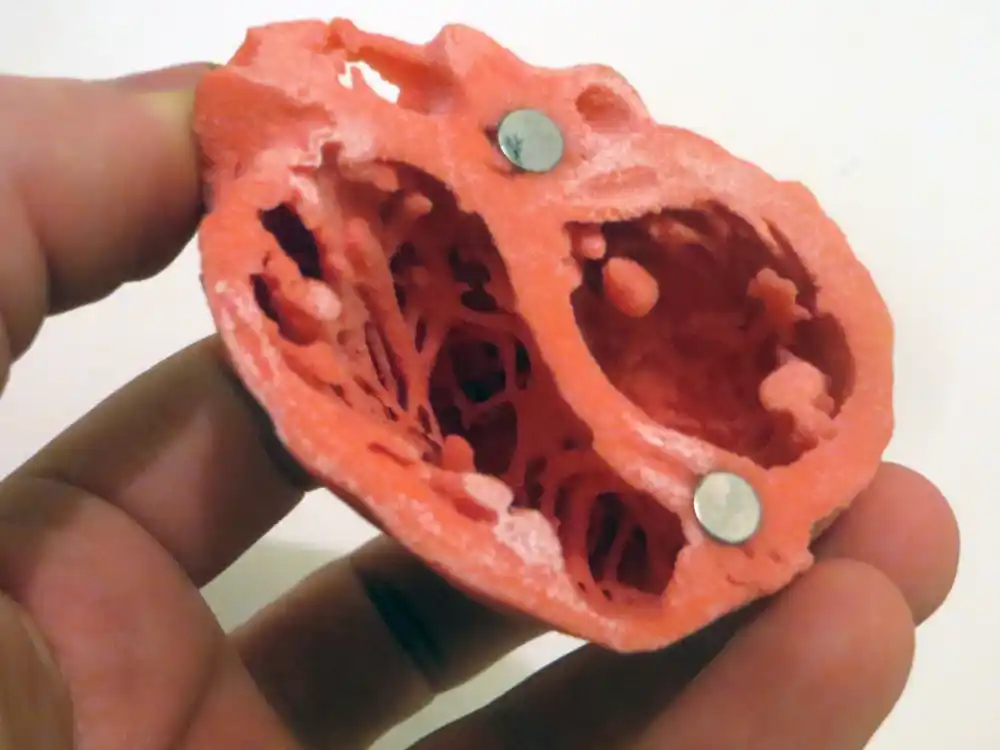
Nakon rođenja, ljudsko srce skoro u potpunosti gubi regenerativnu sposobnost. Oštećenje srčanog mišića — na primer, usled srčanog udara — stoga obično dovodi do trajnog gubitka funkcije kod odraslih. Naučnici sa Instituta Maks Plank za istraživanje srca i pluća su sada prvi put na miševima pokazali da promena u energetskom metabolizmu ćelija srčanog mišića omogućava regeneraciju srca.
Kod životinja bi se funkcija srca mogla u velikoj meri obnoviti nakon srčanog udara. Studija, objavljena u časopisu Nature, revolucionarna je i mogla bi omogućiti potpuno nove terapijske pristupe.
Gubitak regenerativnog kapaciteta srca odraslih je, između ostalog, posledica gubitka sposobnosti ćelija srčanog mišića da se podele nakon rođenja. Ovo je praćeno fundamentalnom promenom u energetskom metabolizmu srčanih ćelija: umesto dobijanja energije iz šećera, što je poznato kao glikoliza, ćelije srčanog mišića sada dobijaju energiju uglavnom iz masti. Ovaj oblik proizvodnje energije poznat je kao oksidacija masnih kiselina.
Istraživačka grupa koju je predvodio Tomas Braun, direktor Instituta Maks Plank za istraživanje srca i pluća u Bad Nauhajmu, Nemačka, počela je da traži nove metode za promovisanje regeneracije srca. „Poznato je da životinjske vrste sposobne da regenerišu svoje srce prvenstveno koriste šećere i glikolizu kao gorivo za ćelije srčanog mišića. I ljudsko srce prvenstveno koristi glikolizu u ranim fazama razvoja, ali onda prelazi na oksidaciju masnih kiselina jer može proizvesti više energije “, objašnjavaju Ksiang Li i Ksuejun Iuan, autori studije.
„Sa prelaskom u proizvodnju energije nakon rođenja, aktivnost mnogih gena se menja i aktivnost deobe ćelija se gubi. Pojedinačni metaboliti iz proizvodnje energije takođe imaju važne funkcije za aktivnost enzima koji regulišu aktivnosti gena. Stoga smo se nadali da ćemo pokrenuti promene u genu. aktivnosti reprogramiranjem energetskog metabolizma kako bi se ponovo uključila sposobnost deljenja ćelija u ćelijama srčanog mišića.“
Da bi to uradili, istraživači Maksa Planka prvo su inaktivirali gen nazvan Cpt1b, koji je neophodan za oksidaciju masnih kiselina, kod miševa. „Potom smo primetili da su srca kod ovih miševa ponovo počela da rastu“, objašnjava Li. Tokom eksperimenta, broj ćelija u srcima ovih miševa se skoro udvostručio. U sledećem koraku, istraživači iz Bad Nauhajma izazvali su srčani udar kod miševa u kojima je Cpt1b bio isključen.
U izabranom pristupu, nakon faze nedostatka dotoka krvi u srce sledi faza reperfuzije, u kojoj se srce ponovo ispira oksigeniranom krvlju. „Ovaj model je uporediv sa srčanim pacijentom čije se srce leči umetanjem stenta zbog okluzije koronarnih arterija“, objašnjava Juan. Efekat je bio impresivan: inače uobičajeni ožiljci na srčanom mišiću bili su jedva primetni posle nedelja, a kontraktilnost kod životinja bez Cpt1b skoro se vratila na nivoe pre infarkta.
U daljim studijama, naučnici su uspeli da dešifruju osnovni mehanizam. „U ćelijama srčanog mišića miševa sa inaktiviranim genom pronašli smo dvadesetostruko povećan nivo alfa-ketoglutarata. Visok nivo ovog metabolita dovodi do značajnog povećanja aktivnosti enzima KDM5“, objašnjava Braun.
Ovaj enzim je takozvana histon demetilaza, koja uklanja metil grupe iz histona i tako smanjuje aktivnost različitih gena. Promena aktivnosti gena dovodi do toga da ćelije srčanog mišića postanu nezrele i tako ponovo steknu sposobnost regeneracije.
Braun vidi studiju kao pravi proboj. „Reprogramiranjem metabolizma udvostručujemo broj ćelija srčanog mišića, a nakon infarkta se funkcija srca skoro potpuno obnavlja. Pored toga, u principu je moguće farmakološki blokirati aktivnost enzima CPT1B – genskog proizvoda Cpt1b. Razvoj inhibitora koji može da se koristi da utiče na aktivnost enzima CPT1B je sledeći korak na putu ka razvoju terapije koja bi se eventualno mogla koristiti kod ljudi.
Međutim, Juan i Braun naglašavaju: „Imamo još dug put pre nego što pouzdani tretmani na ljudima postanu mogući. Primena novih otkrića iz osnovnih istraživanja je dugotrajna i skupa i često je praćena mnogim neočekivanim problemima. Ipak, uvereni smo da ćemo u budućnosti moći terapeutski stimulisati regenerativni kapacitet srca“.