Finija staklena cev i preciznija tehnika sa prefinjenom procedurom mogu da smanje verovatnoću prenošenja mitohondrijalne bolesti tokom potpomognute reprodukcije, prema studiji objavljenoj 5. oktobra u časopisu PLOS Biologi od strane Kifeng Liua i kolega sa Šangajske škole Jiao Tong univerziteta. medicine, Kina. Studija može poboljšati izglede da imaju zdravu bebu za žene koje nose mutacije u svojoj mitohondrijskoj DNK.
Mitohondrije, glavni centar ćelije za proizvodnju energije, imaju sopstvenu DNK koja kodira nekoliko desetina esencijalnih gena. Mutacije u ovim genima mogu izazvati bolest, uključujući vrstu optičke neuropatije, metaboličke poremećaje i bolesti mišića. Ove bolesti se prenose samo preko majke, jer svi mitohondriji embriona potiču iz jajeta, a ne iz sperme.
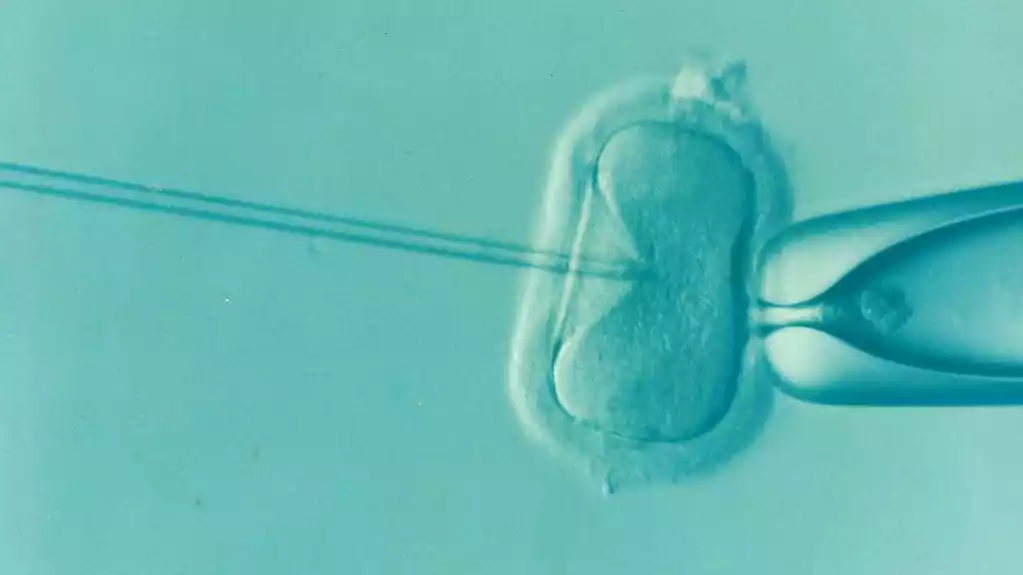
Kod majke koja nosi takve mutacije, jedna tehnika koja se koristi za smanjenje šansi za prenošenje bolesti je transfer vreteno-hromozomskog kompleksa (SCCT), u kojem se nuklearni hromozomi uklanjaju iz neoplođenog jajeta dok su raspoređeni duž strukture koja se zove vreteno. kompleksa, i preneti u jajnu ćeliju donora koja ima zdrave mitohondrije.
Nažalost, neke materinske mitohondrije koje nose bolest često bivaju uništene zajedno sa kompleksom vretena. Posle oplodnje jajeta, tokom formiranja embriona, neki od njih se mogu razmnožavati i formirati značajan deo mitohondrija u nekim tkivima i tako izazvati bolest.
Da bi smanjili verovatnoću prenosa mitohondrija tokom SCCT, autori su napravili tri ključne promene standardnog SCCT protokola. Prvo, preneli su spermu u jajnu ćeliju pre nego što su uklonili vretenasto-hromozomski kompleks, umesto da čekaju do uklanjanja, pošto su prethodne studije pokazale da sama manipulacija može prerano da aktivira mejotski proces, koji je normalno zaustavljen do oplodnje.
Drugo, nakon što su iz jajeta izvukli vretenasto-hromozomski kompleks, prebacili su ga u epruvetu još užeg prečnika (12 mikrometara za miševe, 10 mikrometara za ljude), kako bi počeli da istiskuju citoplazmu iz kompleksa.
Konačno, aspirirali su citoplazmu/kompleks u viskozni hemijski medijum i manipulisali pipetom kako bi dalje odvojili kompleks od citoplazme, proces koji su autori nazvali „odbacivanjem“ nošene citoplazme. Sa kompleksom koji je sada u velikoj meri lišen citoplazme, oni su ga preneli u jajnu ćeliju koja čeka na enukleaciju.
Kod miševa, postupak je rezultirao normalnim razvojem embriona i zdravog potomstva, bez dokaza o ekspanziji mitohondrijalne populacije donora-jajne ćelije u tkivima potomaka. U ljudskim oocitima, nivo mitohondrija prenetih iz jajne ćelije donora bio je oko 4% od onog iz standardnog protokola, bez dokaza o oštećenim hromozomima i visoke stope normalnog ranog embrionalnog razvoja.
„Ovaj novi protokol bi trebalo da smanji prenos mitohondrijalne DNK na najniži mogući nivo“, rekao je Liu, smanjujući rizik od razvoja genetske bolesti kod potomaka majki nosilaca. „Međutim, još nismo mogli da zaključimo da je ova procedura adekvatno bezbedna u klinici za sprečavanje prenošenja naslednih bolesti mitohondrijalne DNK“, a pre kliničkog prevođenja ove procedure biće potrebna dalja istraživanja.
Liu dodaje: „Ističemo da je strategija MRR-SCCT pokazala ne samo efikasno uklanjanje ostataka mtDNK, već i fantastičan razvoj embriona u mišjim i ljudskim oocitima.“