Još uvek postoje mnoge enigme o mehanizmu delovanja gena CERKL, koji izaziva pigmentozu retinitisa i druge nasledne bolesti vida. Sada je tim sa Univerziteta u Barseloni opisao kako nedostatak CERKL gena menja sposobnost ćelija retine da se bore protiv oksidativnog stresa izazvanog svetlošću i pokreće mehanizme ćelijske smrti koji izazivaju slepilo.
Nova studija, objavljena u časopisu Redok Biologi, predstavlja korak napred u karakterizaciji naslednog slepila i identifikaciji ključnih mehanizama za rešavanje budućih tretmana zasnovanih na preciznoj medicini.
Studiju je vodila profesorka Gema Marfani sa Biološkog fakulteta, Instituta za biomedicinu Univerziteta u Barseloni (IBUB) i Biomedicinskog istraživanja umrežavanja retkih bolesti (CIBERER). Istraživačka studija, sprovedena na životinjskim modelima, rezultat je bliske saradnje sa timovima iz Istraživačkog instituta Sant Joan de Deu (IRSJD), Univerziteta u Valensiji, Centra za molekularnu biologiju Severo Ochoa (CSIC-UAM) i bolnice 12 de Octubre Research Institute u Madridu.
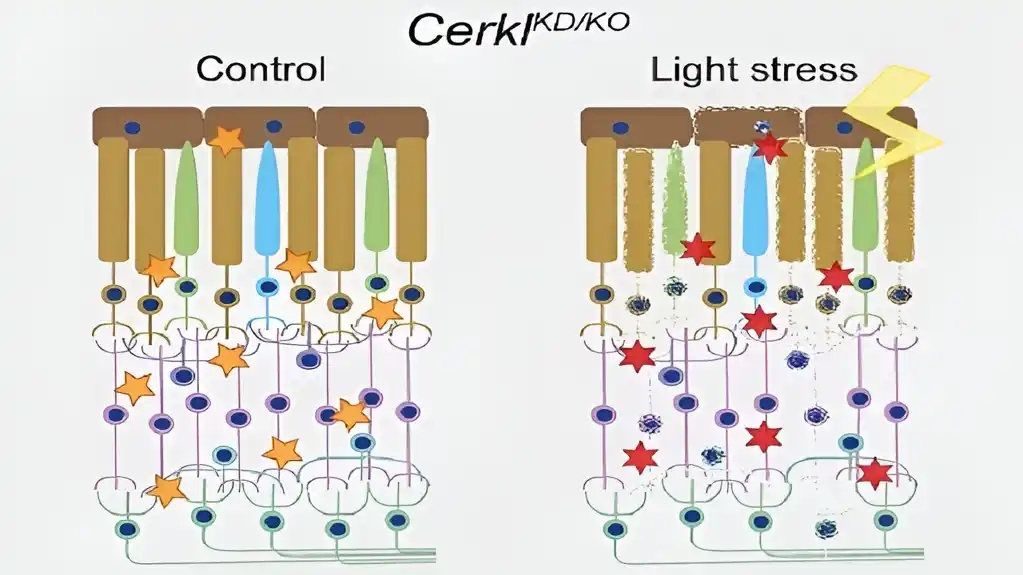
Studija po prvi put otkriva da kada nedostaje CERKL gen, ćelije retine su trajno pod stresom. „Ovo bazalno pogoršano stanje znači da kada se izazove dodatno oksidativno oštećenje – kao kod kontinuirane stimulacije svetlom – ćelije više nisu u stanju da reaguju jer više ne mogu da aktiviraju mehanizme antioksidativnog odgovora“, kaže Marfani, član Odeljenja za genetiku UB. , Mikrobiologija i statistika.
„Zbog toga je retina trajno upaljena. Kao posledica toga, ćelije retine aktiviraju mehanizme ćelijske smrti, kao što su nekroptoza i feroptoza. Iako su eksperimenti izvedeni na miševima, ove promene nam omogućavaju da objasnimo kako i zašto ćelije fotoreceptora umiru kod pacijenata i izazivaju slepilo“, dodaje ona.
Retina je nervno tkivo koje je stalno izloženo svetlosnom stresu — a samim tim i oksidativnom stresu — i ćelije mrežnjače moraju da aktiviraju antioksidativne mehanizme da bi se nosile sa njim. Nova studija je zasnovana na modelu transgenog miša u kojem je gen CERKL eliminisan korišćenjem tehnika za uređivanje gena (CRISPR). Primenom elektrofizioloških tehnika pokazano je da je retina ovih miševa bez CERKL-a progresivno degenerisala na način sličan onom kod ljudi. Ali kako je fiziološka aktivnost izmenjenih fotoreceptora kada je CERKL mutiran?
„Zahvaljujući multidisciplinarnoj saradnji između timova, uspeli smo da kombinujemo različite pristupe kako bismo ušli u patologiju uzrokovanu mutacijama u CERKL. Tehnike transkriptomike su otkrile kako retina reaguje na svetlosni stres kada joj nedostaje CERKL protein. Metabolomska analiza je identifikovala izmenjeni ćelijski biohemijski putevi koji ne dozvoljavaju mrežnjači da se nosi sa oksidativnim oštećenjem izazvanim viškom svetlosti i na kraju izazivaju smrt fotoreceptora“, kaže Marfani.
„Verujemo da je CERKL gen za otpornost na oksidativni stres. Sva ova znanja dopunjuju genetske studije i otvaraju nove puteve za buduće terapijske pristupe“, objašnjava istraživač.
Jedan od 3.000 ljudi u svetu ima neki oblik nasledne distrofije mrežnjače, jednu od retkih bolesti sa najvećom incidencom u populaciji. Do sada je identifikovano ukupno 90 gena povezanih sa retinitis pigmentosa, ali postoji više od 300 gena koji mogu uticati na vid.
„Odlučujuće je da možemo da napravimo dobru genetsku dijagnozu pacijenata i identifikujemo gen koji uzrokuje bolest. Sada znamo da oko 3% pacijenata sa retinitis pigmentosa u Španiji ima mutacije u CERKL genu“, kaže Marfani. „Dobar deo napora u retkim bolestima vida usmeren je upravo na ovu genetsku dijagnozu pacijenata, ali da bi se razumeo fiziološki efekat ovih mutacija potrebno je analizirati šta se dešava u ćelijama mrežnjače.
Identifikovanje gena koji uzrokuje bolest i njegove fiziološke funkcije su kamen temeljac za dizajniranje precizne ili personalizovane terapije. U slučaju genske terapije, ona je obično skupa – u vremenu i novcu – i dostupna samo ograničenom broju pacijenata.
„Sada, ako bolje znamo koji se putevi menjaju kada gen CERKL nedostaje, možemo razmišljati o tome kako da nadoknadimo ove puteve: na primer, lekovima koji mogu da deluju na ove metaboličke puteve i povrate ispravno funkcionisanje neurona mrežnjače i vratite se u homeostatsko stanje. Ova vrsta terapijskog pristupa je mnogo pristupačnija, a ako uspori progresiju bolesti, mogla bi koristiti mnogim pacijentima.“
UB istraživačka grupa za ljudsku molekularnu genetiku ima izvanredne rezultate od više od 25 godina u proučavanju genetske osnove bolesti vida. Bio je vodeći tim u identifikaciji nepoznatog gena — CERKL — kao uzroka pigmentnog retinitisa (The American Journal of Human Genetics, 2004) u studiji porodice sa nekoliko obolele dece.
„Naš tim nastavlja da radi na pokušaju da shvati kako mutacije u CERKL genu uzrokuju smrt fotoreceptora kod pacijenata. U budućnosti, želimo da generišemo nove modele bolesti sa ljudskim retinalnim organoidima, i dizajniramo strategije precizne terapije – gensku terapiju i takođe sa lekovima — zasnovanim na molekulima koji nam omogućavaju da preokrenemo najteže simptome bolesti“, kaže Marfani.