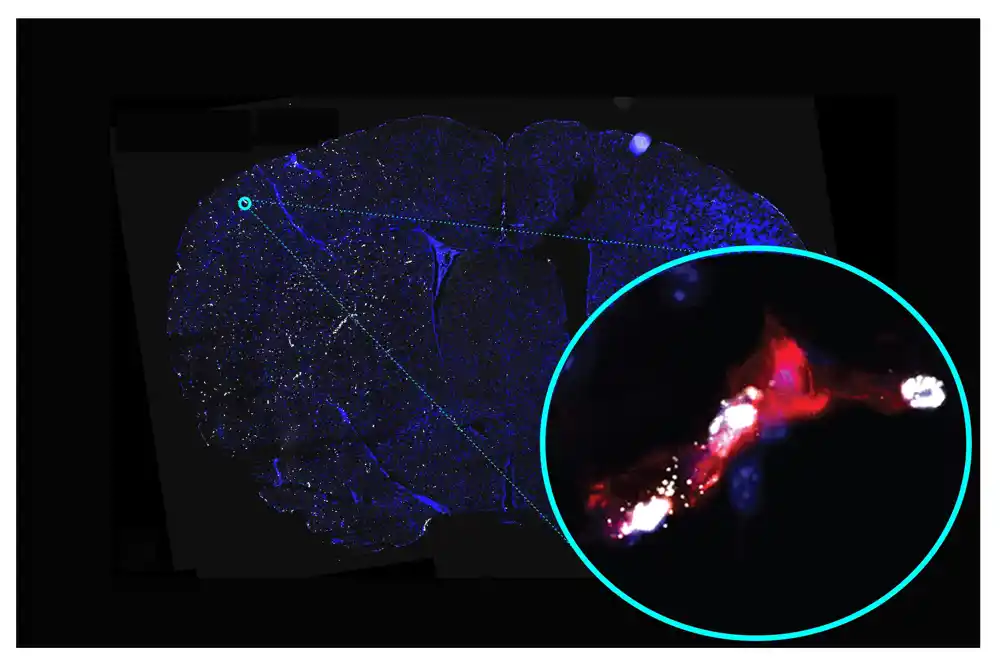
Moždani udari izazivaju brojne promene u genskoj aktivnosti u pogođenim malim krvnim sudovima u mozgu, a ove promene su potencijalno ciljane sa postojećim ili budućim lekovima za ublažavanje povreda mozga ili poboljšanje oporavka od moždanog udara, prema studiji koju su vodili naučnici Veill Cornell Medicine.
U studiji, koja se pojavljuje 14. aprila u Proceedings of the National Academi of Sciences, istraživači su izvršili sveobuhvatno istraživanje, u pretkliničkom modelu, promena aktivnosti gena u malim krvnim sudovima u mozgu nakon moždanog udara. Upoređujući ove promene sa onima koje su zabeležene kod pacijenata sa moždanim udarom, oni su katalogizirali stotine gena sa značajnim promenama izazvanim moždanim udarom i verovatno relevantnim za ljudske moždane udare.
„Naši nalazi pružaju bazu znanja koja poboljšava naše razumevanje moždanog udara i ukazuje na specifične molekule i puteve koji se sada mogu istražiti kao potencijalne mete za buduće tretmane moždanog udara“, rekla je viši autor studije dr Tereza Sančez, docent patologije i laboratorijske medicine. i glavni istraživač Laboratorije za molekularna i translaciona vaskularna istraživanja u Veill Cornell Medicine. „Takođe se sve više priznaje da je vaskularna bolest povezana i doprinosi kognitivnoj disfunkciji i demenciji. Ova studija je identifikovala molekularne karakteristike povezane sa vaskularnom disfunkcijom u ljudskom mozgu nakon moždanog udara, što je glavni uzrok demencije.“
Moždani udar je i dugo je bio vodeći uzrok smrtnosti i dugotrajne invalidnosti širom sveta. Velika većina moždanih udara su ishemijski moždani udari koji uključuju krvni ugrušak u sudu koji služi mozgu. Blokada ili ozbiljno smanjenje protoka krvi smanjuje isporuku kiseonika i hranljivih materija u nizvodne moždane ćelije, ubijajući ih ili povređujući ih i pokrećući zapaljenske procese koji mogu izazvati dalje oštećenje.
Mali cerebralni krvni sudovi – ili „cerebralna mikrovaskulatura“ – nizvodno od blokade su takođe pogođeni, a smatra se da promene u njima dodatno doprinose oštećenju mozga nakon moždanog udara. Ipak, ove mikrovaskularne promene su bile tehnički izazovno tačno zabeležiti, i stoga nisu tako dobro proučene kao drugi aspekti moždanog udara – niti imaju bilo kakav poseban tretman.
U novoj studiji, dr Sančez i njen tim, uključujući prve autore dr. Keri Callegari, Sabiasachi Dash i Hiroki Uchida, koristili su najnovije optimizovane metode, koje je nedavno objavila Sanchez laboratorija u Nature Protocols, za proučavanje krvnih sudova zahvaćenih moždanim udarom kako bi prevazišli ove izazove. Oni su sveobuhvatno zabeležili promene u aktivnosti gena nakon moždanog udara u cerebralnoj mikrovaskulaturi kod miševa i identifikovali promene koje su takođe primećene u studijama pacijenata sa moždanim udarom kod ljudi.
Sveukupno, tim je pronašao 541 gen čija je aktivnost bila promenjena na sličan način i kod miševa i kod ljudskih moždanih krvnih sudova nakon moždanog udara. Podelivši ove gene u grupe na osnovu njihovih funkcionalnih uloga i veza sa bolestima, identifikovali su nekoliko glavnih klastera. Ovo uključuje klastere koji se odnose na opštu upalu, upalu mozga, vaskularnu bolest i vrstu vaskularne disfunkcije koja bi prouzrokovala da cerebralni mikrosudovi propuštaju. Ova nepropusnost podrazumeva slabljenje „krvno-moždane barijere“, ćelijske obloge cerebralnih mikrosudova koja štiti mozak tako što drži većinu komponenti cirkulišuće krvi iz njega.
„Otkrili smo da su, nakon moždanog udara, neki molekuli koji bi oslabili krvno-moždanu barijeru povećani, dok su drugi koji bi trebalo da štite krvno-moždanu barijeru smanjeni“, rekao je dr Sančez, koji je takođe docent neuronauke u Porodični institut za istraživanje mozga i uma Feil. „Ovo je u skladu sa kliničkim zapažanjima poremećaja krvno-moždane barijere nakon moždanog udara.“
Analiza je takođe identifikovala poremećaj normalne aktivnosti u genima koji kontrolišu nivoe sfingolipida. Ovi molekuli povezani sa mastima su u velikoj meri uključeni u regulaciju krvnih sudova, a poremećaji njihovog normalnog rada primećeni su kod moždanog udara, ateroskleroze i vaskularne demencije. Tim je otkrio da su neke vrste ovih sfingolipida visoko obogaćene cerebralnim krvnim sudovima u poređenju sa moždanim tkivom. Pored toga, identifikovali su promene u ovim sfingolipidima u cerebralnoj mikrovaskulaturi izazvane moždanim udarom, kao i promene u ključnim molekulima koji kontrolišu nivoe ovih lipida. Ovi novi nalazi će omogućiti farmakološko ciljanje ovih puteva za terapijsko otkriće moždanog udara.
Studija je uključivala procene koje potvrđuju „pogodnost za lekove“, ili pogodnost za ciljanje sa lekovima sa malim molekulima, mnogih molekula sa izmenjenom produkcijom nakon moždanog udara. Zaista, neki od identifikovanih molekula već su ciljani lekovima kandidatima za lečenje drugih patoloških stanja, što bi moglo olakšati prenamenu ovih lekova za lečenje moždanog udara i demencije.
Doktorka Sančez i njen tim sada prate pretkliničke eksperimente koristeći lekove kandidate ili genetske metode kako bi preokrenuli neke od specifičnih mikrovaskularnih promena identifikovanih u njihovoj studiji, kako bi istražili da li bi to moglo biti korisno za pacijente sa moždanim udarom.
„Stvorili smo ovu platformu znanja i koristimo je, ali se takođe nadamo da će nam se drugi naučnici pridružiti u ovim naporima da razvijemo prve terapije koje ciljaju na mikrovaskulaturu u moždanom udaru“, rekla je ona.