Novi model veštačke inteligencije koji su osmislili istraživači sa Harvardske medicinske škole i Nacionalnog univerziteta Čeng Kung na Tajvanu mogao bi da donese preko potrebnu jasnoću lekarima koji daju prognoze i odlučuju o tretmanima za pacijente sa kolorektalnim karcinomom, drugim najsmrtonosnijim rakom na svetu.
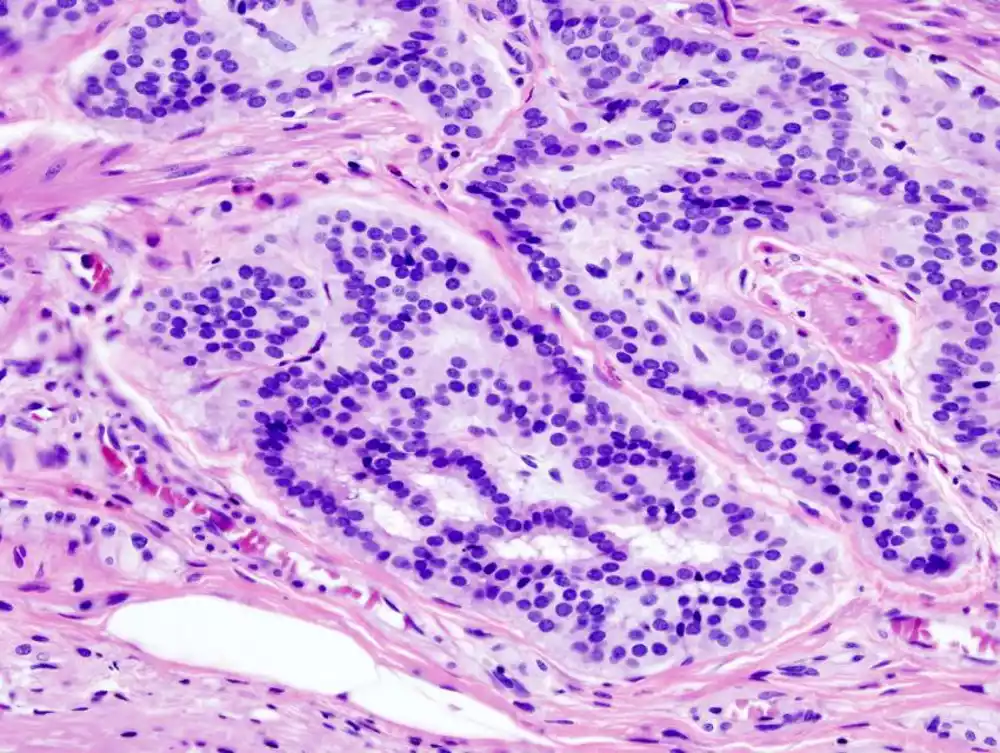
Isključivo gledajući slike uzoraka tumora – mikroskopske prikaze ćelija raka – novi alat tačno predviđa koliko je kolorektalni tumor agresivan, kolika je verovatnoća da će pacijent preživeti sa i bez recidiva bolesti i koja bi optimalna terapija mogla biti za njih.
Izveštaj o radu tima objavljen je u Nature Communications.
Posedovanje alata koji odgovara na takva pitanja moglo bi da pomogne kliničarima i pacijentima da se snađu u ovoj lukavoj bolesti, koja se često ponaša drugačije čak i među ljudima sa sličnim profilima bolesti koji primaju isti tretman – i na kraju bi mogla da poštedi neke od milion života koje karcinom debelog creva iznosi svake godine. .
Istraživači upozoravaju da je alat namenjen da poboljša, a ne da zameni ljudsku stručnost.
„Naš model obavlja zadatke koje ljudski patolozi ne mogu da urade samo na osnovu gledanja slike“, rekao je jedan od viših autora studije Kun-Hsing Iu, docent biomedicinske informatike na Institutu Blavatnik u HMS-u. Ju je predvodio međunarodni tim patologa, onkologa, biomedicinskih informatičara i kompjuterskih naučnika.
„Ono što očekujemo nije zamena ekspertize ljudske patologije, već povećanje onoga što ljudski patolozi mogu da urade“, dodao je Ju. „U potpunosti očekujemo da će ovaj pristup povećati trenutnu kliničku praksu upravljanja rakom.“
Istraživači upozoravaju da prognoza svakog pojedinačnog pacijenta zavisi od više faktora i da nijedan model ne može savršeno predvideti opstanak bilo kog pacijenta. Međutim, dodaju oni, novi model bi mogao biti koristan u usmeravanju kliničara da pažljivije prate, razmatraju agresivnije tretmane ili preporučuju klinička ispitivanja koja testiraju eksperimentalne terapije ako njihovi pacijenti imaju lošije prognoze na osnovu procene alata.
Alat bi mogao biti posebno koristan u oblastima sa ograničenim resursima kako u ovoj zemlji tako i širom sveta gde napredna patologija i genetsko sekvenciranje tumora možda nisu lako dostupni, primetili su istraživači.
Novi alat prevazilazi mnoge trenutne AI alate, koji prvenstveno obavljaju zadatke koji repliciraju ili optimizuju ljudsku stručnost. Novi alat, za poređenje, otkriva i tumači vizuelne obrasce na mikroskopskim slikama koje su nevidljive ljudskom oku.
Alat, nazvan MOMA (za multi-omics Multi-cohort Assessment) je besplatno dostupan istraživačima i kliničarima.
Model je obučen na osnovu informacija dobijenih od skoro 2.000 pacijenata sa kolorektalnim karcinomom iz različitih nacionalnih kohorti pacijenata koje zajedno uključuju više od 450.000 učesnika – Studija praćenja zdravstvenih radnika, Zdravstvena studija medicinskih sestara, Program Atlas genoma raka i NIH-a. PLCO (probno ispitivanje raka prostate, pluća, kolorektalnog i jajnika).
Tokom faze obuke, istraživači su modelu davali informacije o starosti, polu, stadijumu raka i ishodima. Takođe su mu dali informacije o genomskim, epigenetskim, proteinskim i metaboličkim profilima tumora.
Zatim su istraživači pokazali slike modela patologije uzoraka tumora i zatražili od njega da potraži vizuelne markere vezane za tipove tumora, genetske mutacije, epigenetske promene, progresiju bolesti i preživljavanje pacijenata.
Istraživači su zatim testirali kako bi model mogao da funkcioniše u „stvarnom svetu“ tako što su mu dali niz slika uzoraka tumora različitih pacijenata koje ranije nisu videli. Uporedili su njegov učinak sa stvarnim ishodima pacijenata i drugim dostupnim kliničkim informacijama.
Model je tačno predvideo ukupni opstanak pacijenata nakon dijagnoze, kao i koliko od tih godina će biti bez raka.
Alat je takođe tačno predvideo kako bi pojedinačni pacijent mogao da reaguje na različite terapije, na osnovu toga da li pacijentov tumor sadrži specifične genetske mutacije koje su rak učinile manje ili više sklonim progresiji ili širenju.
U obe ove oblasti alat je nadmašio ljudske patologe, kao i trenutne AI modele.
Istraživači su rekli da će model biti podvrgnut periodičnoj nadogradnji kako se nauka bude razvijala i pojavljivali novi podaci.
„Ključno je da sa bilo kojim AI modelom stalno pratimo njegovo ponašanje i performanse jer možemo videti promene u distribuciji tereta bolesti ili novih toksina iz životne sredine koji doprinose razvoju raka“, rekao je Ju. „Važno je dopuniti model novim i više podataka kako se pojavljuju tako da njegove performanse nikada ne zaostaju.
Novi model koristi prednosti nedavnog napretka u tehnikama snimanja tumora koje nude nivoe detalja bez presedana, koji ipak ostaju neprimjetni za ljudske evaluatore. Na osnovu ovih detalja, model je uspešno identifikovao indikatore koliko je tumor bio agresivan i koliko je verovatno da će se ponašati kao odgovor na određeni tretman.
Na osnovu same slike, model je takođe precizirao karakteristike povezane sa prisustvom ili odsustvom specifičnih genetskih mutacija — nešto što obično zahteva genomsko sekvenciranje tumora. Određivanje sekvence može biti dugotrajno i skupo, posebno za bolnice u kojima takve usluge nisu rutinski dostupne.
Upravo u takvim situacijama model bi mogao pružiti pravovremenu podršku pri odlučivanju za izbor tretmana u okruženjima sa ograničenim resursima ili u situacijama kada nema dostupnog tumorskog tkiva za genetsko sekvenciranje, rekli su istraživači.
Istraživači su rekli da pre primene modela za upotrebu u klinikama i bolnicama, treba ga testirati u prospektivnom, randomizovanom ispitivanju koje procenjuje performanse alata kod stvarnih pacijenata tokom vremena nakon početne dijagnoze. Takva studija bi pružila demonstraciju mogućnosti modela kao zlatni standard, rekao je Ju, direktnim upoređivanjem stvarnih performansi alata koristeći samo slike sa ljudskim kliničarima koji koriste znanje i rezultate testova kojima model nema pristup.
Još jedna snaga modela, kažu istraživači, je njegovo transparentno rezonovanje. Ako kliničar koji koristi model pita zašto je napravio dato predviđanje, alat bi mogao da objasni svoje rezonovanje i varijable koje je koristio.
Ova karakteristika je važna za povećanje poverenja kliničara u AI modele koje koriste, rekao je Iu.
Model je precizno odredio karakteristike slike koje se odnose na razlike u preživljavanju.
Na primer, identifikovao je tri karakteristike slike koje su predstavljale lošije ishode:
Model je takođe identifikovao obrasce unutar tumorske strome koji su ukazivali za koje pacijente je veća verovatnoća da će duže živeti bez ponovnog pojave raka.
Alat je takođe tačno predvideo koji pacijenti će imati koristi od klase tretmana raka poznatih kao inhibitori imunoloških kontrolnih tačaka. Dok ove terapije deluju kod mnogih pacijenata sa rakom debelog creva, neke ne doživljavaju nikakvu merljivu korist i imaju ozbiljne neželjene efekte. Model bi tako mogao pomoći kliničarima da prilagode tretman i poštede pacijente koji ne bi imali koristi, rekao je Iu.
Model je takođe uspešno otkrio epigenetske promene povezane sa kolorektalnim karcinomom. Poznato je da ove promene – koje se dešavaju kada se molekuli poznati kao metil grupe vežu za DNK i menjaju kako se ta DNK ponaša – utišavaju gene koji potiskuju tumore, što dovodi do brzog rasta kancera. Sposobnost modela da identifikuje ove promene označava još jedan način na koji može da informiše izbor lečenja i prognozu.