Molekuli ribonukleinske kiseline (RNK) prisutni su u svim živim ćelijama, pri čemu različite vrste RNK imaju različite poslove. Na primer, mesindžer RNK se kopira iz DNK i nosi uputstva o tome kako da se napravi protein. Transfer RNK (tRNK) povezuje sekvencu mRNK sa odgovarajućom amino kiselinom, obezbeđujući da su proteini pravilno spojeni zajedno prema instrukcijama DNK.
Ćelije prirodno modifikuju RNK molekule kako bi poboljšale njihovu stabilnost, strukturu i funkciju. Kada ovaj proces modifikacije krene naopako, to može imati važne posledice po ljudsko zdravlje i bolest. U slučaju tRNK, netačne ili nedostajuće modifikacije proizvode neispravne ili nepotpune proteine, pri čemu je disregulacija modifikacija tRNK povezana sa različitim ljudskim bolestima, uključujući neurodegenerativne bolesti, metaboličke bolesti i rak.
tRNK su molekuli „bogati informacijama“ sa ogromnim potencijalom za dijagnozu i prognozu bolesti, ali do sada nisu bili eksploatisani u te svrhe zbog nedostatka metoda koje bi ove informacije mogle uhvatiti na kvantitativan i isplativ način. Na primer, neke vrste karcinoma je teško dijagnostikovati jer su njihovi simptomi nespecifični i mogu se pomešati sa drugim stanjima. Istovremeno, poznato je da određeni profili modifikacije tRNA postoje samo u specifičnim tipovima raka i mogu poslužiti kao visokospecifični biomarkeri.
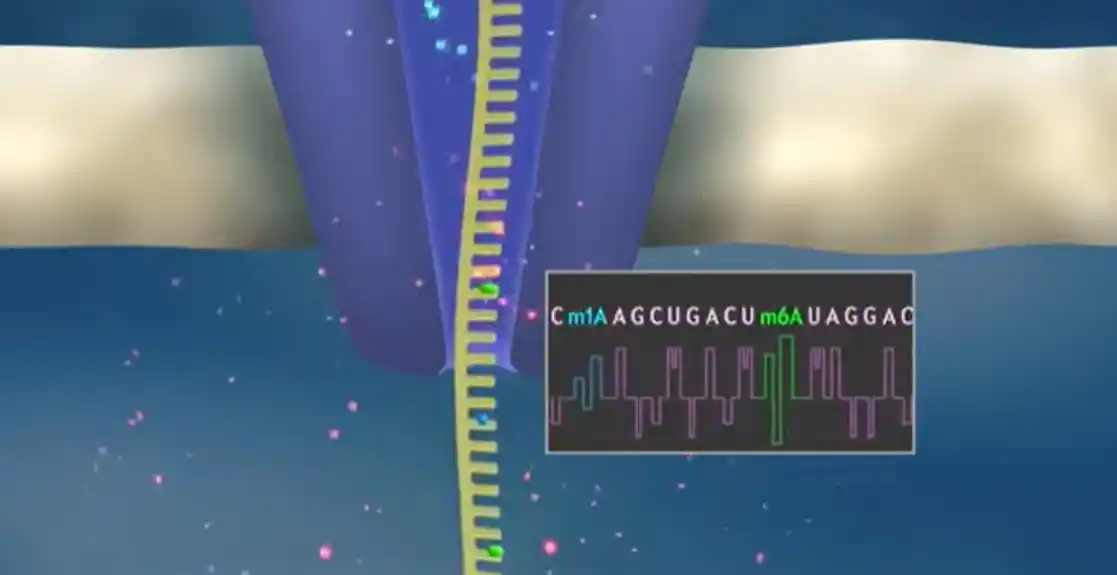
Mogućnost da se izoluju tRNA molekuli iz uzoraka krvi i kvantifikuju njihove modifikacije može pomoći u dijagnostici raka bez upotrebe testova snimanja ili invazivnih biopsija. Štaviše, tip modifikacija tRNK može da se promeni u zavisnosti od stanja bolesti, pružajući vredne informacije o prognozi stanja. Nano-tRNAsek se zasniva na sekvenciranju nanopora, tehnologiji koja može direktno sekvencirati pojedinačne RNK molekule propuštajući ih kroz male pore. Svaki od nukleotida koji čine molekul RNK ima malo drugačiju veličinu i oblik, sa odgovarajućom promenom električne struje koja se javlja kako svaki nukleotid prolazi kroz pore. Kompjuterski programi detektuju promene u struji da identifikuju sekvencu molekula RNK, uključujući sve modifikacije. Zasluge: Eva Novoa/Centar za genomsku regulaciju (CRG)
Trenutne metode za merenje tRNA molekula obično uključuju tehnike kao što su sekvenciranje sledeće generacije ili masena spektrometrija, međutim, ove metode imaju ograničenu upotrebu u dijagnostičke svrhe jer ili nisu u stanju da otkriju modifikacije, ili ne mogu da identifikuju na kojoj lokaciji tRNK se nalaze javlja se u.
Istraživači u Centru za genomsku regulaciju (CRG) u Barseloni su se pozabavili ovim izazovom tako što su razvili novu metodu koja može meriti i obilje i modifikaciju tRNA molekula u jednom koraku. Metoda se zove Nano-tRNAsek i prvi put je opisana danas u časopisu Nature Biotechnologi.
Nano-tRNAsek se zasniva na sekvenciranju nanopora, tehnologiji koja može direktno sekvencirati pojedinačne RNK molekule propuštajući ih kroz male pore. Svaki od nukleotida koji čine molekul RNK ima malo drugačiju veličinu i oblik, sa odgovarajućom promenom električne struje koja se javlja kako svaki nukleotid prolazi kroz pore. Kompjuterski programi detektuju promene u struji da identifikuju sekvencu molekula RNK, uključujući sve modifikacije. Kao dokaz koncepta, istraživači su koristili Nano-tRNAsek za precizno merenje obilja tRNA i modifikacija u uzorcima uzetim iz ćelija kvasca izloženih različitim uslovima životne sredine.
Metoda ima značajne prednosti u odnosu na konvencionalne tehnike. „Prvi put možemo istovremeno da proučavamo i obilje tRNK i profile modifikacije tRNK. Kao bonus, metoda je brza, isplativa, ima visoku propusnost i ima rezoluciju jednog molekula. Ranije smo se oslanjali na dve odvojene metode koji su, zajedno, manje informativni, a za dobijanje rezultata bile bi potrebne nedelje i koštale bi hiljade evra. Nano-tRNAsek je samo delić cene, a rezultate možemo imati u roku od nekoliko dana, au bliskoj budućnosti, u roku od nekoliko sati“, kaže Morgan Lukas, dr. kandidat u Centru za genomsku regulaciju i prvi autor studije.
Brza analiza podataka koju omogućava ovaj metod je kritična za donošenje kliničkih odluka. Još jedna prednost je to što su mašine za sekvenciranje nanopora koje su potrebne za tehniku male, lagane i mogu se napajati pomoću laptopa ili prenosive baterije, što ih čini lakim za transport na udaljene lokacije i omogućavaju upotrebu na terenu ili u klinici.
Istraživači primećuju da još uvek postoje neka ograničenja za novu metodu, kao što je nemogućnost da se predvidi koja modifikacija tRNK je disregulisana u datom uzorku osim ako precizne modifikacije pronađene u toj tRNK nisu prethodno identifikovane korišćenjem drugih eksperimentalnih metoda. „Dok su profili modifikacije tRNA nižih eukariotskih vrsta, kao što je kvasac, dobro okarakterisani, to nije slučaj za ljude. Korišćenjem Nano-tRNAsek-a paralelno sa drugim metodama, možemo opisati profile modifikacije kompletnog skupa humanih tRNA i, u budućnosti, koristite Nano-tRNAsek da identifikujete koje promene u tRNK su povezane sa datom ljudskom bolešću“, dodaje Morgan Lukas.
„Molekuli tRNA se mogu pocepati na male, ali stabilne RNK fragmente koji cirkulišu u krvnoj plazmi. Ovi molekuli se obično menjaju kod pacijenata sa rakom i veoma su bogati informacijama za dijagnostičke i prognostičke svrhe. Nano-tRNAsek je tehnologija koja je dokaz koncepta to otvara put za razvoj jednostavne, isplative i visoko precizne metode koja može kvantifikovati ove molekule na neinvazivan način. Naš cilj je da dalje razvijamo ovu tehnologiju i kombinujemo je sa alatima veštačke inteligencije za određivanje maligniteta biološkog uzorka za manje od 3 sata, a po ceni ne više od 50 evra po uzorku“, kaže dr Eva Novoa, viši autor studije i istraživač u Centru za genomsku regulaciju.