Inhibitor malog molekula koji napada teško ciljanu mutaciju gena KRAS koja izaziva rak, pronađenu u skoro 30 procenata svih tumora kod ljudi, uspešno je smanjio tumore ili zaustavio rast raka u pretkliničkim modelima raka pankreasa, pokazali su istraživači iz Abramsonovog centra za rak pankreasa Penn Medicine, što sugeriše da je lek jak kandidat za klinička ispitivanja. Studija je objavljena danas u Cancer Discoveri.
„Rezultati ove studije su u potpunoj suprotnosti sa bilo čim što smo ranije videli kod raka pankreasa“, rekao je ko-korespondent stariji autor Ben Stanger, MD, Ph.D., profesor Hanna Vise u istraživanju raka u Perelman školi Medicina na Univerzitetu u Pensilvaniji i direktor Centra za istraživanje raka pankreasa Penn. „Čak i u pretkliničkim modelima istraživanja za ovaj tip raka, većina lekova testiranih u poslednjoj deceniji – uključujući nove imunoterapije – imala je ograničen uticaj.“
Pacijenti sa rakom pankreasa imaju opštu lošu prognozu sa petogodišnjom stopom preživljavanja od 11 procenata i ograničenim mogućnostima lečenja. Skoro 90 procenata karcinoma pankreasa uzrokovano je mutacijom KRAS gena, najčešćeg onkogena među tipovima raka. Prva ciljana terapija za KRAS odobrena je prošle godine za rak pluća ne-malih ćelija sa KRAS G12C mutacijama, ali samo 2 procenta karcinoma pankreasa izražava tu vrstu mutacije. Oko 36 procenata karcinoma pankreasa sa KRAS mutacijom je KRAS G12D-mutant.
Inhibitor malih molekula koji se koristi u ovoj studiji, MRTKS1133 (razvijen od strane Mirati Therapeutics) posebno cilja na KRAS G12D, kao što je kompanija prvi put objavila prošlog meseca u Nature Medicine. Pennova studija sada pokazuje da KRAS-inhibitor ne samo da direktno cilja ćelije raka, već i neočekivano sarađuje sa imunološkim sistemom kako bi proizveo trajni odgovor na lečenje, što je važno jer rak na kraju pronađe način da izbegne većinu ciljanih terapija.
„Iz studija KRAS G12C i drugih studija ciljane terapije znamo da će se rezistencija dogoditi“, rekao je Stanger. „Čak i pre nego što dođemo do kliničkih ispitivanja, razmišljamo o tome kako da kombinujemo lekove tako da se tumori ne vrate. Naši nalazi pružaju dokaze koji sugerišu imunoterapiju kao partnera sa KRAS G12D inhibitorima.“
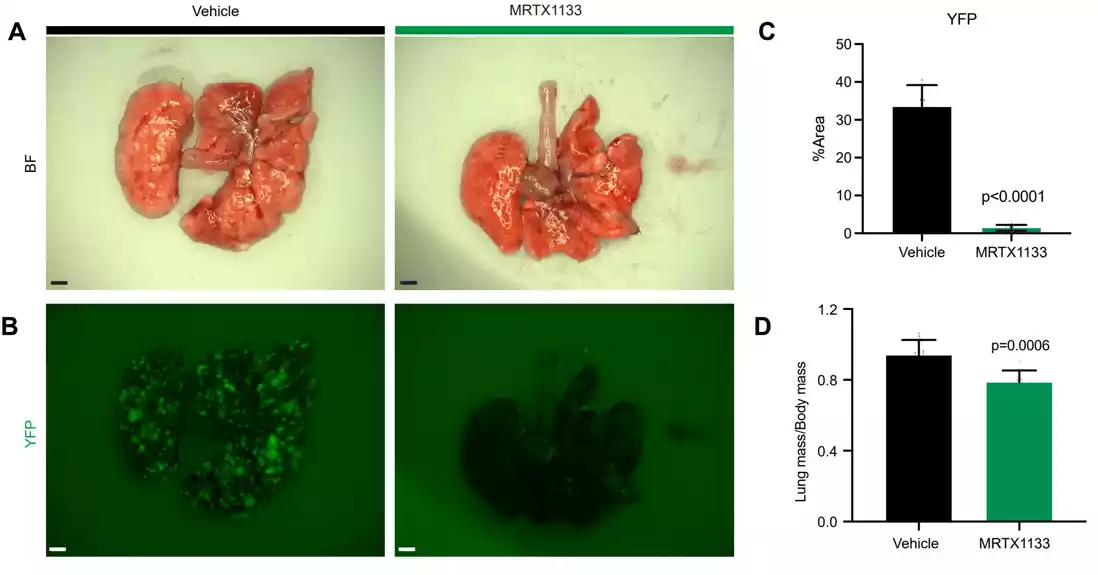
Istraživači su bili u mogućnosti da procene uticaj MRTKS1133 na imuni sistem jer tip modela koji se koristi u studiji omogućava tumoru da spontano evoluira nakon implantacije kod inače zdravih miševa, što omogućava da se uoči uticaj leka na okolno mikrookruženje tumora ( TME).
Imunokompetentni KPC model je razvio Penn Medicine pre skoro 20 godina i predstavlja zlatni standard koji se koristi širom sveta za procenu potencijalnih terapija za duktalni adenokarcinom pankreasa (PDAC). PDAC je poznat po tome što ima posebno gust TME, što doprinosi otpornosti na terapiju.
Istraživački tim je otkrio da je lek podstakao povećanje T ćelija u TME, što je poboljšalo dubinu i trajanje odgovora na MRTKS1133. Sve potpune remisije uočene u studiji bile su praćene antitumorskim imunitetom posredovanim T ćelijama. Kod miševa bez T ćelija, efekat MRTKS1133 je bio kratak i tumori rastu mnogo brže. Ovi rezultati sugerišu da se MRTKS1133 može kombinovati sa imunoterapijom kako bi se poboljšao dugoročni odgovor na terapiju i sprečio povratak raka.
„Posle mnogo godina rada na pronalaženju preko potrebnih novih pristupa za pacijente sa rakom pankreasa, uzbudljivo je imati novu klasu lekova na horizontu“, rekao je ko-korespondent Robert Vonderheide, MD, DPhil, direktor Abramsonovog raka. Centar i profesor Centra za rak John H. Glick Abramson na Medicinskom fakultetu Perelman, čiji su članovi laboratorije radili sa onima u Stangerovoj laboratoriji u fokusiranom kooperativnom timu na ovoj studiji.
„Optimisti smo da će KRAS G12D inhibitori uskoro ući u klinička ispitivanja. KRAS se predaje i sada znamo da imuni sistem to može da vidi.“